─┐Ū░Ż¼╬ęć°ą┬ą═├║╗»╣żŲ¾śI░lš╣čĖ╦┘Ż¼ų„ę¬╝»ųąį┌├║╠┐┘Yį┤žSĖ╗Īó╦«┘Yį┤Č╠╚▒Ą─╬„▒▒Ąžģ^Ż¼║─╦«┴┐┤¾Ą─═¼ĢrÅU╦«┼┼Ę┼┴┐Š▐┤¾Ż¼ÅU╦«ų▒Įė┼┼Ę┼Ģ■ŲŲē─╦«¾wŁhŠ│ĪŻ▓╔├║╩ĶĖ╔╦«ų„ę¬ųĖ├║╠┐ķ_▓╔▀^│╠ųąŠ«Ž┬Ąž┘|ąįė┐ØB╦«ĄĮŽ’Ą└Īó×ķ░▓╚½╔·«aČ°┼┼│÷Ą─ūį╚╗ĄžŽ┬╦«║═Š«Ž┬▓╔├║╔·«a▀^│╠ųą×ó╦«ĪóĮĄēmĪó£ń╗╣ÓØ{ĪóŽ¹Ę└╝░ę║ē║įOéõ«a╔·Ą─ÅU╦«Ż¼ō■Įyėŗ╬ęć°├┐─Ļ╩ĶĖ╔╦«┼┼Ę┼┴┐Ė▀▀_45Ī┴108m3ĪŻę“┤╦Ż¼ī”╩ĶĖ╔╦«▀Mąą╠Ä└Ē▓ó╝ėęįŠC║Ž└¹ė├Ż¼▓╗āH┐╔ęįėąą¦ĮŌøQ║─╦«┴┐┤¾Ą─å¢Ņ}Ż¼═¼ĢrŻ¼Įø▀^▀Mę╗▓Į╔ŅČ╚╠Ä└Ē║¾┐╔ū„×ķ╣żśIė├╦«Īó▐rśI╣ÓĖ╚ė├╦«╗“ĄžŽ┬╦«čaĮoŻ¼▒▄├Ō┴╦╦«┘Yį┤Ą─└╦┘MĪŻ
╩ĶĖ╔╦«Ą─╦«┘|╠žąįų„ę¬╩▄Ąž┘|Śl╝■Īó├║īė╠žąįĪó▓╔├║╣ż╦ćĄ─ė░ĒæŻ¼ų„ę¬║¼ėą¤oÖC¹}ŅÉĪóųžĮī┘Īó╣╠¾wŅw┴Ż║═╬ó╔·╬’Ą╚ĪŻŲõųąŻ¼¤oÖC¹}ŅÉ░³└©SO42-ĪóCl-ĪóNO3-ĪóCa2+ĪóMg2+Ą╚ĪŻ═¼ĢrŻ¼ė╔ė┌├║Ę█║═ÄrĘ█ØB╚ļ╦«ųąą╬│╔Ą─Ė▀æęĖĪ╣╠¾wŻ©SSŻ®Ż¼╦«Ą─Ņü╔½ę╗░Ń│╩╗ę╔½ĪŻ╩ĶĖ╔╦«ę╗░ŃąĶę¬Įø▀^ę╗ŽĄ┴ąĄ─╬’└ĒĪó╗»īW║═╔·╬’╠Ä└ĒŻ¼▓┼─▄▀_ĄĮ╗žė├ś╦£╩ĪŻĄ½╩ŪŲõųąė▓Č╚ļxūėĄ─┤µį┌Ż©ę╗░Ńį┌500~2000mg/Lų«ķgŻ¼ęįCaCO3ėŗŻ®Ż¼Ģ■į÷╝ė║¾└m╠Ä└ĒŽĄĮy╣▄Ą└Ą─ĮY╣Ė’LļUŻ¼ė░Ēæ╔ŅČ╚╠Ä└ĒŁh╣Ø─żĄ─╩╣ė├ē█├³ĪŻę“┤╦Ż¼╩ĶĖ╔╦«═∙═∙ąĶꬎ╚Įø▀^▄ø╗»╚ź│²ŲõųąĄ─ė▓Č╚ļxūė║¾Ż¼▓┼─▄▀Mę╗▓Į╠Ä└Ē┼c╗žė├ĪŻ
─┐Ū░Ż¼│Żė├Ą─╦«¾w▄ø╗»ĘĮĘ©ų„ę¬ėą╬³ĖĮĘ©Īó─żĘųļxĘ©ĪóļŖ╗»īWĘ©Īó╗»īW│┴ĄĒĘ©Ą╚ĪŻŲõųąŻ¼╬³ĖĮĘ©╦«┴”═Ż┴¶Ģrķg▌^ķLŻ¼─żĘųļxĘ©▀mė├ė┌Ą═ė▓Č╚╦«╠Ä└ĒŻ¼ļŖ╗»īWĘ©ąĶꬎ¹║─┤¾┴┐ļŖ┴”Ż¼─▄║─Ė▀ĪŻČ°╗»īW│┴ĄĒĘ©ę“Ųõ╝╝ąg│╔╩ņĪó▓┘ū„║åå╬Č°▒╗ÅVĘ║æ¬ė├Ż¼Ą½╩ŪĢ■«a╔·┤¾┴┐Ą─║¼╦«╬█─ÓŻ¼ąĶĮY║Žē║×Vå╬į¬╩╣ė├Ż¼į÷╝ė┴╦š╝Ąž├µĘe║═╠Ä└Ē│╔▒ŠŻ¼į┌┤╦▀^│╠ųąŻ¼æęĖĪ╬’ę▓Ą├ĄĮ┴╦═¼▓Į╚ź│²Č°ūā│╔║¼╦«╬█─ÓĪŻę“Č°Ż¼žĮĒÜķ_░lę╗ĘNĖ▀ą¦ĪóĄ═║─ĪóČ╠┴„│╠Ą─ÅU╦«ė▓Č╚╠Ä└Ē╝╝ągŻ¼īŹ¼Fī”ė▓Č╚ļxūėĄ─Ė▀ą¦╚ź│²Ż¼═¼ĢrĮĄĄ═│÷╦«ØßČ╚ĪŻ╗∙ė┌┤╦Ż¼šnŅ}ĮMčą░l┴╦║╦Š¦įņ┴ŻŻ©NCPŻ®╝╝ągŻ¼įOėŗ▓ó║Ž│╔┴╦Ō}ĪóµVļxūėīŻė├Š¦ĘNŻ¼ķ_░l┴╦ę╗¾w╗»čbéõĪŻŠ▀¾wĄžŻ¼įō╝╝ąg═©▀^ŅAŽ╚Ž“čbéõųą═Č╝ėę╗Č©┴┐Ą─īŻė├Š¦ĘNŻ¼š{š¹╦Ää®═Č╝ė┴┐Ż¼╩╣Ą├Ō}ĪóµVļxūėĘųäeęį╠╝╦ßŌ}ĪóÜõč§╗»µVĄ─ą╬╩ĮĮYŠ¦ė┌īŻė├Š¦ĘN╔ŽŻ¼═¼Ģr═©▀^š{š¹╦«┴”īWģóöĄŻ¼īŹ¼Fī”ė▓Č╚ļxūė║═æęĖĪ╬’Ą─═¼▓Į╚ź│²Ż¼▓óą╬│╔ų┬├▄Ą─įņ┴Ż¾wŻ¼¤oąĶ╬█─Ó├ō╦«ĪŻ
ęįā╚├╔╣┼─│ĄVśI╣½╦Š▓╔├║╩ĶĖ╔╦«×ķ蹊┐ī”Ž¾Ż¼Į©┴ó┴╦ųąįć╠Ä└ĒŽĄĮyŻ¼▓ó▓╔ė├2╝ē┤«┬ōĄ─║╦Š¦įņ┴Ż╝╝ągŻ¼╠ĮŠ┐▓╗═¼╣ż╦ćģóöĄŚl╝■Ž┬ī”ė▓Č╚ļxūė┼cæęĖĪ╬’Ą─╚ź│²ą¦┬╩Ż¼═¼Ģrī”įņ┴Ż¾w▀Mąą▒Ēš„Ęų╬÷Ż¼Įę╩Š║╦Š¦įņ┴Ż═¼▓Į╚ź│²ÖC└ĒŻ¼ęįŲ┌×ķ║¾└mĄ─╣ż│╠æ¬ė├╠ß╣®ę└ō■ĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 ųąįć╦«┘|
ųąįćį┌ā╚├╔╣┼קīÅŲņ─│ĄVśI╣½╦Š▀MąąŻ¼▓╔├║╩ĶĖ╔╦«Įø▀^š{╣Ø│žĪóą▒░Õ│┴ĄĒ│ž╚ź│²╦«ųą┤¾Ņw┴ŻĄ─│┴ĄĒ╬’║¾▀M╚ļ║╦Š¦įņ┴ŻįOéõĪŻĮø£yČ©Ż¼pH×ķ8.25Ī└0.13Ż¼TDS×ķŻ©7760Ī└230Ż®mg/LŻ¼┐éė▓Č╚Ż©ęįCaCO3ėŗŻ®×ķŻ©1310.3Ī└100.5Ż®mg/LŻ¼Ca2+×ķŻ©344Ī└12.5Ż®mg/LŻ¼Mg2+×ķŻ©105.6Ī└10.2Ż®mg/LŻ¼HCO3-×ķŻ©552Ī└20.3Ż®mg/LŻ¼ØßČ╚×ķŻ©65.38Ī└8.35Ż®NTUĪŻė╔ė┌įŁ╦«pHį┌8.2ū¾ėęŻ¼ę“┤╦¤oąĶš{š¹pHŻ¼┐╔ęįų▒Įė▀M╚ļ║╦Š¦įņ┴ŻĘ┤æ¬Ų„ĪŻ
1.2 įć“×▓─┴Ž
ųąįćųąŻ¼ę╗╝ē╩╣ė├Ō}ĪóµVīŻė├Å═║ŽŠ¦ĘNŻ¼Č■╝ē╩╣ė├µVīŻė├Š¦ĘNŻ¼ā╔ĘNŠ¦ĘNĄ─│§╩╝┴ŻÅĮŠ∙×ķ80~120─┐Ż©0.15~0.2mmŻ®Ż¼ę“┤╦Š▀ėą▌^┤¾Ą─▒╚▒Ē├µĘeŻ¼▀@×ķCa2+/Mg2+Ą─ĖĮų°│╔║╦╠ß╣®┴╦Ė³ČÓ╬╗³cĪŻŲõųąŻ¼Ō}īŻė├Š¦ĘNĄ─Čč├▄Č╚╝s×ķ1.5g/cm3Ż¼µVīŻė├Š¦ĘNĄ─Čč├▄Č╚╝s×ķ1.2g/cm3Ż¼Ė▀├▄Č╚Ą─Š¦ĘN╠ßĖ▀┴╦Ųõ─═ø_ō¶žō║╔Ą──▄┴”Ż¼═¼Ģr─▄ē“┐ņ╦┘│┴ĮĄĪŻė╔ė┌įŁ╦«ųą║¼ėą┤¾┴┐Ą─HCO3-Ż¼ę“┤╦Ż¼Ą┌ę╗╝ē┼cĄ┌Č■╝ē║╦Š¦įņ┴ŻŠ∙╩╣ė├NaOHū„×ķšTŠ¦ä®ĪŻ
1.3 ųąįćčbų├
¼Fł÷ųąįćčbų├╚ńłD1╦∙╩ŠŻ¼Ę┤æ¬Ų„ų„¾wė╔SS304▓╗õPõō╝ė╣żČ°│╔Ż¼┐éĖ▀×ķ6.0mŻ¼ė╔Ąū▓┐ų┴Ēö▓┐Ęų×ķĘ┤æ¬ģ^Ż©1.2mŻ®Īóįņ┴Żģ^Ż©3.0mŻ®║═Ęųļxģ^Ż©1.8mŻ®Ż╗įOéõĄū▓┐įOėą▀M╦«┐┌║═▀M╦Ä┐┌ĪŻį┌▒├Ą─ū„ė├Ž┬įŁ╦«▀M╚ļĄ┌ę╗╝ēĘ┤æ¬Ų„Ż¼═¼Ģr▀M╦Ä▒├īóNaOH╦═╚ļĘ┤æ¬Ų„│²Ō}Ż¼Ą┌ę╗╝ēĘ┤æ¬ĮY╩°║¾│÷╦«▀M╚ļųąķg╦«ŽõŻ¼į┘Įøė╔▒├▀M╚ļĄ┌Č■╝ēĘ┤æ¬Ų„Ż¼═¼Ģr╝ė╚ļNaOHė├ęį│²µVĪŻĘ┤æ¬ĮY╩°║¾Ż¼š{╣Ø│÷╦«pHų┴ųąąįĪŻųąįć▀^│╠ųąŻ¼Ą┌ę╗╝ē╠Ä└Ē─▄┴”×ķ22m3/hŻ¼Ą┌Č■╝ē╠Ä└Ē─▄┴”×ķ10m3/hĪŻ▓┐ĘųĄ┌ę╗╝ē│÷╦«▒╗╗ž┴„ų┴įŁėą╦«╠Ä└ĒŽĄĮyŻ¼ī”ųąįć▓╗«a╔·ė░ĒæĪŻ
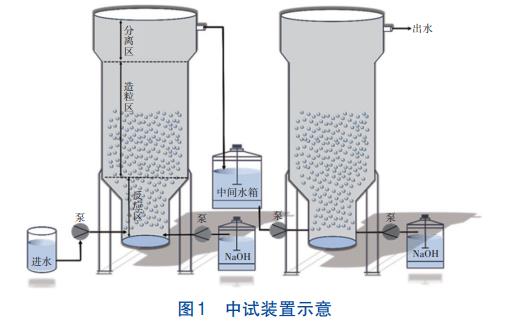
1.4 Ęų╬÷āxŲ„┼cĘĮĘ©
pHŻ║ŖW║└╦╣ST3100ą═pHėŗŻ╗┐éė▓Č╚ĪóŌ}ĪóµVļxūėŻ║ć°ś╦EDTAĄ╬Č©Ę©Ż╗ØßČ╚Ż║╣■╝{HI93703-11ØßČ╚āxŻ¼ų▒Įė£yČ©│÷╦«Ż╗įņ┴Żą╬├▓╝░į¬╦žĘų▓╝▒Ēš„Ż║Ą┬ć°ZEISSSigma300SEM─▄ūVāxŻ©SEMŻ®Ż╗▒Ē├µ╗∙łFĪ󊦹═ĮYśŗĘų╬÷Ż║╚š▒ŠŹuĮ“IRTracer100ą═ĖĄ└’╚~┬■Ę┤╔õ╝t═Ō╣ŌūVāxŻ©FT-IRŻ®Īó├└ć°ThermoScientificESCALABXią═X╔õŠĆ╣ŌļŖūė─▄ūVāxŻ©XPSŻ®║═Ą┬ć°BrukerD8Advanceeą═X╔õŠĆč▄╔õāxŻ©XRDŻ®Ż╗įņ┴Ż¾w┴ŻÅĮŻ║ėóć°±RĀ¢╬─Mastersizer2000ą═╝ż╣Ō┴ŻČ╚āxĪŻŌ}ĪóµVļxūė╚ź│²┬╩Ą─ėŗ╦ŃĘĮĘ©╚ńŽ┬Ż║
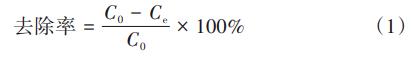
╩ĮųąŻ║C0×ķ▀M╦«Ō}ĪóµVļxūėØŌČ╚Ż╗Ce×ķ│÷╦«Įøš{š¹│╔ųąąį║¾Ą─Ō}ĪóµVļxūėØŌČ╚ĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 ║╦Š¦įņ┴Ż╝╝ągī”Ō}ĪóµVļxūėĄ─╚ź│²┬╩
ā╔╝ē┤«┬ō║╦Š¦įņ┴Ż╝╝ągī”Ō}ĪóµVļxūėĄ─╚ź│²ą¦╣¹╝░ØßČ╚ė░ĒæęŖłD2ĪŻ
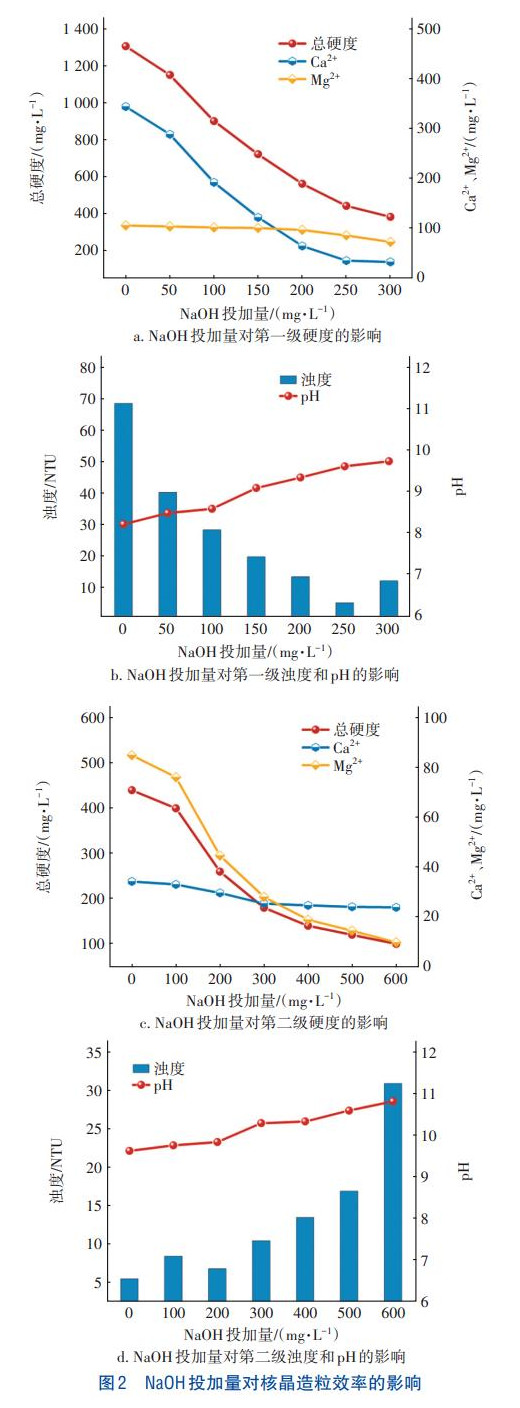
«öÅU╦«ųąĄ─ļxūėØŌČ╚Ęe┤¾ė┌CaCO3Ą─╚▄Č╚ĘeŻ©KspŻ®ĢrŻ¼CaCO3Ģ■ę“×ķ▀^’¢║═Č°ĮYŠ¦╬÷│÷Ż¼MgŻ©OHŻ®2ę▓╩Ū╚ń┤╦ĪŻę“┤╦Ż¼▀^’¢║═Č╚╩Ū“īäėļxūėĮYŠ¦╬÷│÷Ą─ų„ę¬äė┴”ĪŻė╔ė┌įŁ╦«ųą┤µį┌╝s550mg/LŻ©9.01mmol/LŻ®HCO3-Ż¼└Ēšō╔Ž┼cNaOHĘ┤æ¬─▄ē“╔·│╔9.01mmol/LCO32-Ż¼┐╔┼c╝s360mg/LĄ─Ca2+Ę┤æ¬╔·│╔CaCO3Ż¼ę“┤╦Ż¼Ą┌ę╗╝ē║╦Š¦įņ┴ŻĘ┤æ¬Ų„ųą¤oąĶŅ~═Ō╝ė╚ļNa2CO3ĪŻ╚ńłD2Ż©aŻ®╦∙╩ŠŻ¼ļSų°NaOH═Č╝ė┴┐Ą─į÷╝ėŻ¼┐éė▓Č╚║═Ca2+ØŌČ╚│╩¼F├„’@Ž┬ĮĄ┌ģä▌Ż¼Ą½╩ŪMg2+ØŌČ╚Ž┬ĮĄ▓╗├„’@ĪŻ▀@╩Ūė╔ė┌┤╦ĢrNaOH┼cHCO3-Ę┤æ¬╔·│╔┴╦CO32-Ż¼▀MČ°┼cCa2+Ę┤æ¬╔·│╔CaCO3Č°ĮYŠ¦ė┌Ō}īŻė├Š¦ĘN╔ŽĪŻČ°┤╦ĢrĄ─pH╝░NaOH═Č╝ė┴┐▓╗ūŃęį▀_ĄĮMgŻ©OHŻ®2│┴ĄĒĄ─▀^’¢║═Č╚ĪŻę“┤╦Mg2+Ą─╚ź│²┐╔─▄╩Ūė╔ė┌╣▓│┴ĄĒū„ė├ĪŻ
ė╔łD2Ż©bŻ®┐╔ų¬Ż¼ļSų°NaOH═Č╝ė┴┐Ą─į÷╝ėŻ¼│÷╦«ØßČ╚Ž╚ĮĄĄ═║¾į÷╝ėŻ¼«öNaOH═Č╝ė┴┐×ķ250mg/LĢrØßČ╚▀_ĄĮūŅĄ═Ż©5.6NTUŻ®Ż¼┤╦Ģrī”┐éė▓Č╚ĪóCa2+ĪóMg2+║═ØßČ╚Ą─╚ź│²┬╩Ęųäe×ķ66.3%Īó90.1%Īó19.0%║═91.8%ĪŻ«ö═Č╝ė┴┐└^└mį÷╝ėų┴300mg/LĢrŻ¼┐éė▓Č╚ĪóCa2+║═Mg2+Ą─╚ź│²┬╩╚įį┌į÷╝ėŻ¼Ą½│÷╦«ØßČ╚├„’@╔Ž╔²Ż¼▀@╩Ūė╔ė┌╔·│╔Ą─CaCO3║═MgŻ©OHŻ®2▓ó╬┤ĮYŠ¦ĖĮų°ė┌Ō}īŻė├Š¦ĘN╔ŽŻ¼Č°╩ŪļS│÷╦«┴„│÷ĪŻ
ė╔łD2Ż©cŻ®┐╔ų¬Ż¼ļSų°NaOH═Č╝ė┴┐Ą─į÷╝ėŻ¼ī”┐éė▓Č╚║═Mg2+Ą─╚ź│²ą¦╣¹├„’@╠ßĖ▀Ż¼▀@╩Ūė╔ė┌┤╦Ģrų„ę¬╔·│╔┴╦MgŻ©OHŻ®2ĮYŠ¦▓óĖĮų°ė┌µVīŻė├Š¦ĘN╔ŽĪŻŌ}ļxūėätė╔ė┌╣▓│┴ĄĒū„ė├Č°▒╗╔┘┴┐╚ź│²ĪŻĄ½╩Ū▓╗═¼ė┌Ą┌ę╗╝ē║╦Š¦įņ┴ŻŻ¼ļSų°NaOH═Č╝ė┴┐Ą─į÷╝ėŻ¼│÷╦«ØßČ╚│╩¼FųØu╔Ž╔²┌ģä▌Ż¼▀@┐╔─▄╩Ū╦«ųą┤µį┌╔┘┴┐Ca2+Ż¼ė░Ēæ┴╦MgŻ©OHŻ®2Ą─ĖĮų°Ż¼ī¦ų┬│÷╦«ØßČ╚╔Ž╔²ĪŻę“┤╦Ż¼ŠC║Ž┐╝æ]│÷╦«ė▓Č╚Ż©<200mg/LŻ®┼cØßČ╚Ż¼┤_Č©Ą┌Č■╝ē║╦Š¦įņ┴ŻĄ─╝ė╦Ä┴┐×ķ500mg/LĪŻ╩┬īŹ╔ŽŻ¼īó│÷╦«š{╣Øų┴ųąąį║¾Ż¼┐éė▓Č╚╝s×ķ140mg/LŻ¼─▄ē“ØMūŃ│÷╦«ų«ė┌ė▓Č╚ę¬Ū¾ĪŻūŅĮKŻ¼Įøė╔Ą┌ę╗ĪóĄ┌Č■╝ē║╦Š¦įņ┴Ż╠Ä└Ē║¾Ż¼┐éė▓Č╚ĪóCa2+ĪóMg2+║═ØßČ╚Ą─╚ź│²┬╩Ęųäe▀_ĄĮ┴╦91.1%Īó93.1%Īó86.3%║═75.3%ĪŻ
2.2 Š¦ĘN╠Ņ│õ┘|┴┐Īó╔Ž╔²┴„╦┘ī”│÷╦«╦«┘|Ą─ė░Ēæ
▓╗═¼Š¦ĘNė├┴┐Ž┬Ż¼Ė„ųĖś╦Ą─╚ź│²ą¦╣¹ęŖłD3ĪŻ
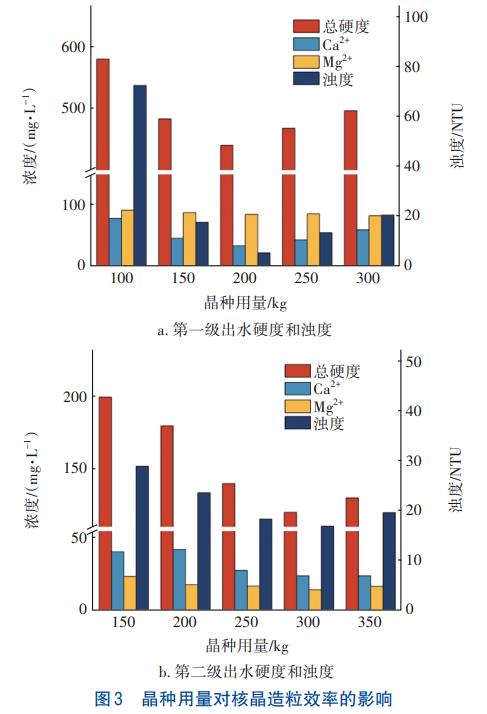
į┌Ą┌ę╗╝ē║╦Š¦įņ┴ŻįOéõųąŻ¼ļSų°īŻė├Š¦ĘNė├┴┐Ą─į÷╝ėŻ¼│÷╦«ė▓Č╚ĪóCa2+ØŌČ╚║═ØßČ╚Š∙│╩¼FŽ╚£pąĪ║¾į÷╝ėĄ─┌ģä▌Ż¼Č°Mg2+ØŌČ╚Äū║§ø]░l╔·ūā╗»ĪŻ«öŠ¦ĘNė├┴┐×ķ200kgĢrŻ¼│÷╦«ą¦╣¹▀_ĄĮūŅ╝čĪŻĘų╬÷įŁę“Ż¼«öŠ¦ĘNė├┴┐╔┘ė┌200kgĢrŻ¼ŲõĮYŠ¦─▄┴”▓╗ūŃęį╬³ĖĮ╚½▓┐CaCO3/MgŻ©OHŻ®2Ņw┴ŻŻ¼ī¦ų┬│÷╦«ØßČ╚▌^Ė▀Ż╗Č°«öŠ¦ĘNė├┴┐>200kgĢrŻ¼ė╔ė┌▀M╦«╔Ž╔²┴„╦┘ę╗Č©Ż¼Š¦ĘN┴„╗»ĀŅæBūā▓ŅŻ¼▀MČ°ĮĄĄ═┴╦Š¦ĘN┼cCaCO3/MgŻ©OHŻ®2Ą─Įėė|├µĘeŻ¼ī¦ų┬│÷╦«ØßČ╚╔²Ė▀ĪŻ═¼śėŻ¼┤_Č©Ą┌Č■╝ē║╦Š¦įņ┴ŻĄ─ūŅ╝芦ĘNė├┴┐×ķ300kgĪŻ
│²┤╦ų«═ŌŻ¼╦«┴”Śl╝■ę▓Ģ■ė░Ēæ╬█╚Š╬’į┌Š¦ĘN▒Ē├µĄ─ĖĮų°ĪŻė╔ė┌ųąįćįOéõĄ─│▀┤ń╩Ū╣╠Č©Ą─Ż¼ę“┤╦═©▀^š{š¹▀M╦«┴„┴┐┐╔Ė─ūāŲõ╔Ž╔²╦┘Č╚Ż¼▀MČ°ė░Ēæ╬█╚Š╬’┼cŠ¦ĘNĄ─Įėė|Ģrķg║═Įėė|├µĘeĪóŠ¦ĘNĄ─┴„╗»ĀŅæBęį╝░ŽĄĮyĄ─╗ņ║ŽÅŖČ╚ĪŻ▓╗═¼╔Ž╔²┴„╦┘Ž┬Ż¼ī”┐éė▓Č╚ĪóCa2+ĪóMg2+║═ØßČ╚Ą─╚ź│²ą¦╣¹ęŖłD4ĪŻ
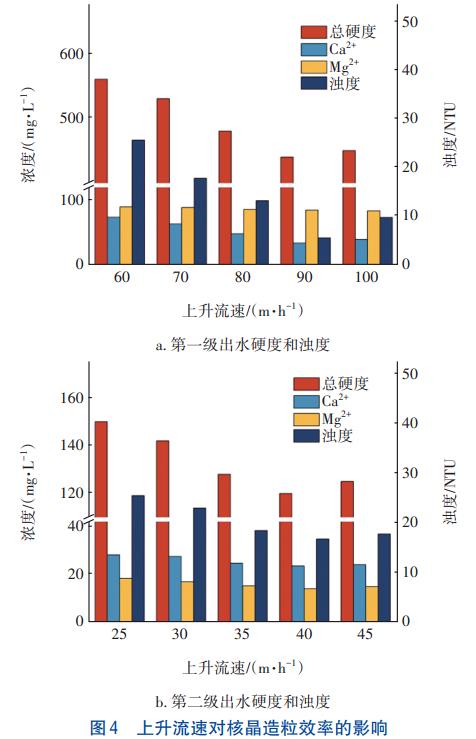
ė╔łD4Ż©aŻ®┐╔ų¬Ż¼«ö╔Ž╔²┴„╦┘×ķ90m/hĢrŻ¼│÷╦«ØßČ╚▀_ĄĮūŅĄ═ųĄŻ¼Č°┤¾ė┌╗“ąĪė┌90m/hĢr│÷╦«ØßČ╚Š∙╔²Ė▀ĪŻĘų╬÷įŁę“Ż¼«ö╔Ž╔²┴„╦┘▌^ąĪĢrŻ¼īŻė├Š¦ĘN▓╗─▄▀_ĄĮūŅ╝č┴„╗»ĀŅæBŻ¼ī¦ų┬Š¦ĘN▒®┬Č╬╗³c╔┘Ż¼ļyęį╩╣CaCO3/MgŻ©OHŻ®2╚½▓┐ĖĮų°ė┌Š¦ĘN╔ŽŻ¼ļS╦«┴„┴„│÷Å─Č°į÷╝ė┴╦│÷╦«ØßČ╚ĪŻČ°▀^Ė▀Ą─╔Ž╔²┴„╦┘Ż¼ļm╚╗Ģ■╩╣Š¦ĘNĄ─┴„╗»ĀŅæBūāĄ├Ė³║├Ż¼Ą½£p╔┘┴╦Š¦ĘN┼c╬█╚Š╬’Ą─Įėė|ĢrķgŻ¼▓óĢ■ø_╦óŠ¦ĘN▒Ē├µĄ─ĖĮų°╬’Ż¼ī¦ų┬│÷╦«ØßČ╚╔²Ė▀ĪŻ═¼śėŻ¼┤_Č©Ą┌Č■╝ē║╦Š¦įņ┴ŻĄ─ūŅ╝č╔Ž╔²┴„╦┘×ķ40m/hĪŻ
2.3 ▀B└mĘĆČ©▀\ąąą¦╣¹
į┌Ęųäe╠ĮŠ┐┴╦Ą┌ę╗ĪóĄ┌Č■╝ē║╦Š¦įņ┴ŻĄ─ė░Ēæę“╦ž╗∙ĄA╔ŽŻ¼▀Mąą┴╦72hĄ─▀B└m┴„įć“ׯ¼ęį“×ūCŽĄĮyĄ─ĘĆČ©ąį╝░─═ø_ō¶žō║╔─▄┴”ĪŻŲõķg├┐Ė¶4h£yČ©▀M╦«║═Ą┌Č■╝ē║╦Š¦įņ┴Ż│÷╦«Ą─┐éė▓Č╚ĪóØßČ╚║═pHŻ¼ĮY╣¹▒Ē├„Ż¼▀M╦«ŲĮŠ∙┐éė▓Č╚║═ØßČ╚Ęųäe×ķ1358.9mg/L║═59.3NTUŻ¼Č°Ą┌Č■╝ē│÷╦«Ą─Ęųäe×ķ140.2mg/L║═18.4NTUŻ¼╚ź│²┬╩Ęųäe×ķ89.7%║═68.9%ĪŻųĄĄ├ūóęŌĄ─╩ŪŻ¼į┌▀B└m▀\ąą▀^│╠ųąŻ¼▀M╦«Ą─┐éė▓Č╚╝░ØßČ╚▓©äė▌^┤¾Ż¼Ą½╩Ū│÷╦«┐éė▓Č╚─▄ē“ØMūŃąĪė┌200mg/LĄ─ę¬Ū¾Ż¼═¼Ģr│÷╦«ØßČ╚▓©äė▌^ąĪŻ¼│÷╦«pHŲĮŠ∙ųĄ×ķ10.58ĪŻę“┤╦Ż¼┐╔ęį┐ŽČ©Ą─╩ŪŻ¼ā╔╝ē┤«┬ōĄ─║╦Š¦įņ┴ŻŽĄĮy─▄ē“═¼▓Į╚ź│²ÅU╦«ųąĄ─ė▓Č╚║═ØßČ╚Ż¼▓ó▒Ē¼F│÷ā׫ɥ─ąį─▄╝░ĘĆČ©ąįĪŻ
2.4 įņ┴Ż¾wą╬├▓ĪóĮM│╔╝░▒Ē├µ╠žąįĘų╬÷
į┌Įø▀^▀B└m72h▀\ąą║¾Ż¼Ęųäe╚Ī│÷Ą┌ę╗ĪóČ■╝ē║╦Š¦įņ┴Żčbų├Ąū▓┐Ą─įņ┴Ż¾wŻ¼ė├ęįĘų╬÷įņ┴Ż¾wĄ─ĮYśŗ╠žš„ĪŻXRDĘų╬÷ĮY╣¹’@╩ŠŻ¼Ą┌ę╗╝ēįņ┴Ż¾wį┌2”╚×ķ26.2ĪŃĪó27.2ĪŃĪó33.1ĪŃĪó37.9ĪŃĪó46.5ĪŃĪó48.9ĪŃĪó51.9ĪŃĪó53.0ĪŃ║═53.9ĪŃ╠Ä│╩¼F│÷├„’@Ą─č▄╔õĘÕŻ¼┼cCaCO3Ą─╠žš„č▄╔õĘÕŠ½£╩╬Ū║ŽŻ©JCPDS#76-0606Ż®Ż¼Ūę¤oŲõ╦¹ļsĘÕŻ¼▀@▒Ē├„į┌Ą┌ę╗╝ē║╦Š¦įņ┴Żčbų├ųąą╬│╔┴╦▌^╝āĄ─CaCO3įņ┴Ż¾wĪŻ═¼śėĄžŻ¼Ą┌Č■╝ēįņ┴Ż¾wį┌2”╚×ķ18.5ĪŃĪó37.9ĪŃĪó50.7ĪŃ║═58.6ĪŃ╠Ä│╩¼F│÷├„’@Ą─č▄╔õĘÕŻ¼▀@┼cMgŻ©OHŻ®2Ą─╠žš„č▄╔õĘÕ╬Ū║ŽŻ©JCPDS#84-2163Ż®Ż¼▒Ē├„į┌Ą┌Č■╝ē║╦Š¦įņ┴Żčbų├ųąą╬│╔┴╦MgŻ©OHŻ®2įņ┴Ż¾wĪŻ│²┤╦ų«═ŌŻ¼MgŻ©OHŻ®2įņ┴Ż¾wXRDłDųą│÷¼F┴╦├„’@Ą─īŻė├Š¦ĘNĄ─╠žš„č▄╔õĘÕŻ¼▀@╩Ūę“×ķĄ┌Č■╝ēįŁ╦«ųąĄ─Mg2+ØŌČ╚▌^Ą═Ż¼╔·│╔Ą─MgŻ©OHŻ®2║¼┴┐Ą═Ż¼▓ó╬┤═Ļ╚½Ė▓╔wīŻė├Š¦ĘNĪŻ
Ą┌ę╗╝ē║═Ą┌Č■╝ē║╦Š¦įņ┴Ż¾wį┌▓╗═¼▒ČöĄŽ┬Ą─SEM║═EDSššŲ¼ęŖłD5ĪŻ┐╔ęį┐┤│÷Ż¼Ą┌ę╗╝ēĄ─CaCO3įņ┴Ż¾w┴ŻÅĮĘų▓╝Š∙ä“Ż¼┴ŻÅĮ┤¾╝s×ķ1.0mmŻ¼▀@ūC├„ÅU╦«ųąĄ─Ca2+ęčĮøęįCaCO3Ą─ą╬╩ĮĖĮų°▓ó╔·ķLė┌īŻė├Š¦ĘN▒Ē├µŻ©Š¦ĘN┴ŻÅĮ╝s×ķ0.2mmŻ®Ż¼▓ó┤┘╩╣Š¦ĘNķL┤¾ĪŻčąŠ┐▒Ē├„Ż¼CaCO3Š¦¾w▒Ē├µ╣Ō╗¼Ż¼Š▀ėąęÄätĄ─ą▒ĘĮ¾w╗“Ū“ą╬ĮYśŗĪŻĄ½╩ŪŻ¼Ą┌ę╗╝ēųąĄ─CaCO3įņ┴Ż¾w▒Ē├µ│╩¼F┤ų▓┌ĀŅŻ¼ĖĮų°┴╦▓╗ęÄätĄ─╬’┘|Ż¼▀@╩Ūė╔ÅU╦«ųąĄ─æęĖĪ╬’▒╗═¼▓Į╚ź│²╦∙ī¦ų┬Ą─ĪŻ═¼śėĄžŻ¼Ą┌Č■╝ēųąĄ─MgŻ©OHŻ®2įņ┴Ż¾w▒Ē├µę▓ĖĮų°┴╦æęĖĪ╬’Ż¼Ą½╩Ūė╔ė┌Mg2+║¼┴┐▌^╔┘Ż¼ę“┤╦Ųõįņ┴Ż¾wāH╩Ū▓┐Ęų│╩¼FęÄätĀŅŻ¼Č°Ūę▓ó╬┤ķL┤¾ĪŻÅ─EDSššŲ¼┐╔ęį┐┤│÷Ż¼CaCO3įņ┴Ż¾w▒Ē├µ║¼ėąMgį¬╦žŻ¼Č°MgŻ©OHŻ®2įņ┴Ż¾w▒Ē├µ║¼ėąCaį¬╦žŻ¼▀@╩Ūė╔ė┌░l╔·┴╦╣▓│┴ĄĒū„ė├Ż¼╩╣Ą├Mg2+║═Ca2+Ęųäe│┴ĄĒė┌CaCO3║═MgŻ©OHŻ®2įņ┴Ż¾w▒Ē├µĪŻ

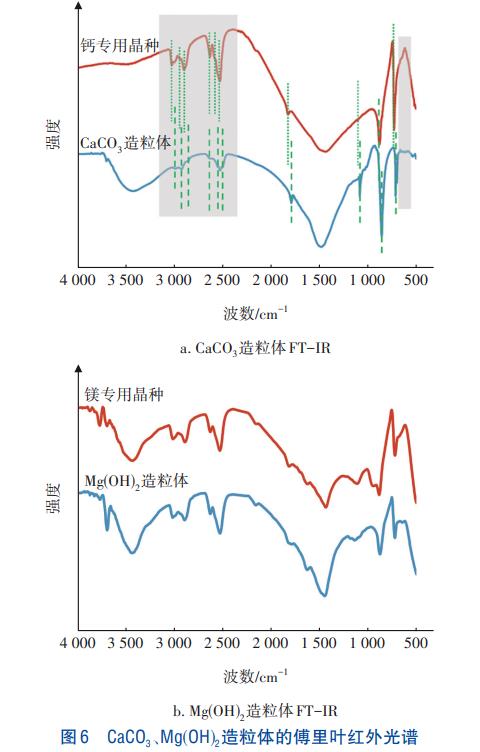
łD6│╩¼F┴╦Ą┌ę╗╝ē║═Ą┌Č■╝ē║╦Š¦įņ┴Ż¾wĄ─ĖĄ└’╚~╝t═Ō╣ŌūVŻ©FT-IRŻ®ĪŻ╚ńłD6Ż©aŻ®╦∙╩ŠŻ¼┐╔ęį├„’@ė^▓ņĄĮŌ}īŻė├Š¦ĘNĄ─č▄╔õĘÕŠ∙ęčĮø▒╗CaCO3įņ┴Ż¾wĄ─č▄╔õĘÕĖ▓╔wŻ¼▀@ūC├„┴╦ÅU╦«ųąĄ─CaCO3ęčĮø╔·ķLį┌Ō}īŻė├Š¦ĘN▒Ē├µŻ¼▓ó┤┘▀MŲõ╔·ķLŻ¼▀@┼cXRDĮY╣¹ę╗ų┬ĪŻ═¼Ģr┐╔ęįė^▓ņĄĮŻ¼ŽÓ▒╚ė┌Ō}īŻė├Š¦ĘNŻ¼CaCO3įņ┴Ż¾wį┌2500~3000cm-1║═500~750cm-1╠ÄĄ─č▄╔õĘÕŽÓī”ŲĮš¹ŪęĖ³╣Ō╗¼Ż¼▀@╩Ūė╔ė┌æęĖĪ╬’Ą─ŪČ╚ļ╩╣Ą├CaCO3╗∙łF┼┼┴ą▓╗ęÄätŻ¼ęįų┬ŽÓÓÅĘÕŽÓ▀BČ°║Ž▓óŻ¼┤┘╩╣╬³╩šÄ¦öĄ─┐£p╔┘Ż¼│╔×ķę╗ą®īÆČ°ŌgĄ─ĦĪŻ▀@▒Ē├„ÅU╦«ųąĄ─æęĖĪ╬’▒╗═¼▓Į╚ź│²Ż¼│²▒╗▒Ē├µ╬³ĖĮ═ŌŻ¼ę▓ŪČ╚ļCaCO3įņ┴Ż¾wųąŻ¼▀@┼cSEMĮY╣¹ę╗ų┬ĪŻĄ½╩ŪŻ¼═¼śėĄ─ĮY╣¹▓ó╬┤│÷¼Fį┌µVīŻė├Š¦ĘN║═MgŻ©OHŻ®2įņ┴Ż¾wĄ─FT-IRłDųąŻ¼▀@ę▓ķgĮėūC├„┴╦µVįņ┴Ż¾wė╔ė┌Mg2+║¼┴┐╔┘Ż¼Č°▓ó╬┤┤┘╩╣īŻė├Š¦ĘNķL┤¾Ż¼ę“┤╦Č■š▀Ą─FT-IRłD▓óø]ėą├„’@ūā╗»ĪŻ
ī”Ą┌ę╗ĪóĄ┌Č■╝ēįņ┴Ż¾wĄ─┴ŻÅĮĘų▓╝£yČ©ĮY╣¹’@╩ŠŻ¼CaCO3įņ┴Ż¾wĄ─d10Īód50Īód90Ęųäe×ķ664.7Īó902.2Īó1322.6”╠mŻ¼├„’@┤¾ė┌īŻė├Š¦ĘNŻ©0.15~0.2mmŻ®Ż¼ūC├„┴╦īŻė├Š¦ĘNķL┤¾ĪŻŽÓĘ┤Ż¼MgŻ©OHŻ®2įņ┴Ż¾wĄ─ŽÓæ¬ųĄĘųäeų╗ėą117.4Īó228.9Īó395.2”╠mŻ¼āH┬į┤¾ė┌µVīŻė├Š¦ĘNĪŻ▀@ę▓┼cSEMĮY╣¹ę╗ų┬ĪŻĄ½╩ŪŻ¼╚ń╣¹ķLŲ┌▀\ąąŻ¼MgŻ©OHŻ®2ūŅĮKĢ■┤┘╩╣µVīŻė├Š¦ĘNķL┤¾Ż¼Å─Č°╩╣Ą├Mg2+Å─ÅU╦«ųą╚ź│²ĪŻ
Ęųäe╚ĪCaCO3ĪóMgŻ©OHŻ®2įņ┴Ż¾wŻ¼£yČ©ŲõX╔õŠĆ╣ŌļŖūė─▄ūVŻ©XPSŻ®Ż¼ė├ęį▀Mę╗▓Į┴╦ĮŌįņ┴Ż¾wĄ─▒Ē├µ╗»īW│╔ĘųŻ¼ĮY╣¹╚ńłD7╦∙╩ŠĪŻī”ė┌CaCO3įņ┴Ż¾wŻ¼XPSĄ─Æ▀├ĶĮY╣¹ūCīŹ┴╦CĪóOĪóCa║═MgĄ─┤µį┌ĪŻłD7Ż©aŻ®ųąŻ¼C1sĄ─Ė▀Ęų▒µ┬╩ĘųĘÕöM║ŽĮY╣¹’@╩Š┴╦╚²éĆ╠╝╦ß¹}ŽÓĻPĄ─ĘÕųĄĪŻŲõųą284.8eV╠Äė^▓ņĄĮ┴╦CĪ¬C/C=OĄ─ĘÕŻ¼┐╔─▄╩ŪÅU╦«ųąĄ─ėąÖC╬’▒╗╬³ĖĮė┌įņ┴Ż¾w╔Ž╦∙ų┬Ż¼▀@ę╗³cęč▒╗Ž╚Ū░Ą─蹊┐ūCīŹĪŻ289.7eV╠ÄĄ─ĮY║Ž─▄ĘÕī”æ¬ė┌╠╝╦ß¹}Ą─ĘÕŻ¼286.3eV╠ÄĄ─ĘÕät┤·▒Ē┴╦ÜłėÓ║¼č§╗∙łFųąĄ─CĪ¬OĪŻŅÉ╦ŲĄžŻ¼O1s┐╔ęį▒╗öM║Ž×ķ╚²éĆĘÕŻ¼ęŖłD7Ż©bŻ®ĪŻŲõųąŻ¼╬╗ė┌533.3eV╠ÄĄ─ĘÕ┤·▒Ē┴╦OĪ¬H/CĪ¬OĪ¬CŻ╗╬╗ė┌531.9eV╠ÄĄ─ĘÕ┤·▒Ē┴╦CaCO3įņ┴Ż¾wųąĄ─CO32-Ż╗Č°╬╗ė┌530.9eV╠ÄĄ─ĘÕät┤·▒Ē┴╦HOĪ¬MgŻ¼▀@▒Ē├„Ųõįņ┴Ż¾w▒Ē├µ┤µį┌MgĪŻ
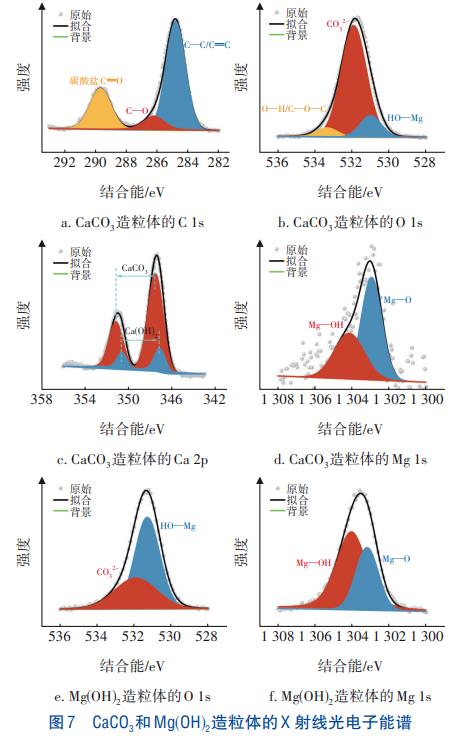
į┌łD7Ż©cŻ®ųąCa2pĘÕ┐╔ęį▒╗ĘųäeöM║Ž×ķ╬╗ė┌315.2Īó347.5eVĄ─CaCO3ęį╝░╬╗ė┌350.6Īó347.1eVĄ─CaŻ©OHŻ®2Ż¼įŁę“┐╔─▄╩ŪNaOHĄ─═Č╝ėī¦ų┬╔·│╔┴╦CaŻ©OHŻ®2ĪŻMg1s┐╔ęį▒╗öM║Ž×ķ╬╗ė┌1304.2eVĄ─MgĪ¬OHĘÕęį╝░1302.9eVĄ─MgĪ¬OĘÕŻ¼▀@ūC├„┴╦CaCO3įņ┴Ż¾w▒Ē├µ┤µį┌MgŻ©OHŻ®2Ż¼Ą½╩Ūę“×ķŲõ║¼┴┐▌^╔┘Č°╬┤į┌XRDųą¾w¼FĪŻį┌łD7Ż©eŻ®ųąŻ¼MgŻ©OHŻ®2įņ┴Ż¾wĄ─O1s┐╔ęį▒╗öM║Ž×ķā╔éĆĘÕŻ¼Ęųäe╩Ū╬╗ė┌531.9eV╠ÄĄ─CO32-ĘÕ║═531.3eV╠ÄĄ─HOĪ¬MgĘÕŻ¼įŁę“┐╔─▄╩Ū╦«ųąÜłėÓĄ─CO32-ī¦ų┬MgŻ©OHŻ®2įņ┴Ż¾w▒Ē├µ┤µį┌CO32-ĪŻČ°Mg1s┐╔ęį▒╗öM║Ž×ķ╬╗ė┌1304.2eV╠ÄĄ─MgĪ¬OHĘÕ╝░╬╗ė┌1302.9eV╠ÄĄ─MgĪ¬OĘÕŻ¼ūC├„┴╦įņ┴Ż¾wĄ─ų„ę¬│╔Ęų×ķMgŻ©OHŻ®2ĪŻę“┤╦Ż¼Įø▀^ī”║╦Š¦įņ┴Ż¾wĄ─ŽĄ┴ą▒Ēš„Ż¼┐╔ęį┤_Č©ÅU╦«ųąĄ─Ca2+ĪóMg2+ęį╝░æęĖĪ╬’▒╗═¼▓Į╚ź│²Ż¼Č°ŪęĘųäeį┌Ą┌ę╗╝ē║═Ą┌Č■╝ē║╦Š¦įņ┴Żčbų├ųąą╬│╔┴╦├▄īŹĄ─CaCO3ĪóMgŻ©OHŻ®2įņ┴Ż¾wĪŻ
2.5 ║╦Š¦įņ┴ŻÖC└ĒĘų╬÷
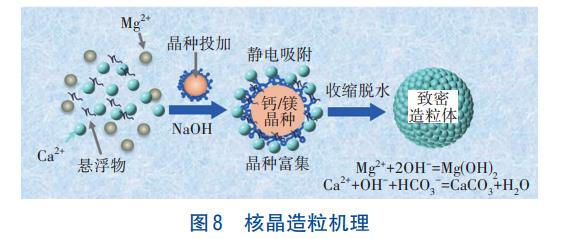
╗∙ė┌╔Ž╩÷▒Ēš„Ęų╬÷Ż¼ÅU╦«ųąCa2+ĪóMg2+Ą─║╦Š¦įņ┴Ż╚ź│²ÖCųŲęŖłD8ĪŻ╩ūŽ╚Ż¼ī”īŻė├Š¦ĘN▒Ē├µZetaļŖ╬╗▀Mąą┴╦Ęų╬÷Ż¼«öpH×ķ3.2Īó6.8Īó8.9Īó9.8Īó10.6Īó11.8ĢrŻ¼Ō}īŻė├Š¦ĘN▒Ē├µZetaļŖ╬╗Ęųäe×ķ5.3Īó-6.2Īó-7.6Īó-5.5Īó-8.3Īó-9.6mVŻ╗«öpH×ķ3.2Īó5.8Īó7.8Īó9.5Īó10.9Īó11.2Īó11.5ĢrŻ¼µVīŻė├Š¦ĘN▒Ē├µZetaļŖ╬╗Ęųäe×ķ4.6Īó1.3Īó-9.8Īó-13.5Īó-14.9Īó-16.8Īó-18.3mVĪŻ┐╔ęŖŻ¼į┌pH>8ĢrŌ}ĪóµVīŻė├Š¦ĘN▒Ē├µŠ∙ĦžōļŖĪŻę“┤╦į┌Ą┌ę╗╝ē║╦Š¦įņ┴Żčbų├ųąŻ¼«öŠ¦ĘN│õĘų┴„╗»║¾Ż¼ÅU╦«ųąĄ─Ca2+ė╔ė┌ņoļŖ╬³ĖĮū„ė├Ż¼Š█╝»ė┌īŻė├Š¦ĘN╔ŽŻ¼┤╦ĢrŻ¼╝ė╚ļĄ─NaOH╠ß╣®┴╦┤¾┴┐Ą─OH-Ż¼▓ó┐ņ╦┘┼cįŁ╦«ųąĄ─HCO3-Ę┤æ¬╔·│╔CO32-Ż¼┼c╬³ĖĮė┌īŻė├Š¦ĘN╔ŽĄ─Ca2+Ę┤æ¬╔·│╔CaCO3Ż¼▀MČ°┤┘╩╣īŻė├Š¦ĘNķL┤¾Ż¼į┌┤╦▀^│╠ųą╣³ÆČ┴╦ÅU╦«ųąĄ─æęĖĪ╬’Ż¼┤┘╩╣Ųõ═¼▓Į╚ź│²ĪŻČ°«öīŻė├Š¦ĘN▒╗Ė▓╔w║¾Ż¼Ųõ▒Ē├µ×ķą┬╔·│╔Ą─CaCO3Ż¼Ūęą┬╔·│╔Ą─CaCO3▒Ē├µ╚įĦžōļŖ║╔Ż¼ę“┤╦Ģ■╬³ĖĮCa2+ĖĮų°Ż¼╚ń┤╦裣h╩╣Ą├īŻė├Š¦ĘNļSų°▀\ąąĢrķLČ°ķL┤¾Ż¼▓óį┌╦«┴”ū„ė├Ž┬├▄īŹ╗»ĪŻ▓╗═¼Ą─╩ŪŻ¼į┌Ą┌Č■╝ē║╦Š¦įņ┴Żčbų├ųąŻ¼│§╩╝ė╔ė┌ņoļŖū„ė├Ż¼Mg2+▒╗╬³ĖĮė┌īŻė├Š¦ĘN▒Ē├µŻ¼NaOHĄ─╝ė╚ļ╩╣Ą├MgŻ©OHŻ®2╠Äė┌▀^’¢║═ĀŅæBŻ¼Å─Č°į┌Š¦ĘN▒Ē├µ▓╗öÓ▀MąąĖ╗╝»Ż¼▓ó┤┘╩╣ŲõķL┤¾ĪŻČ°«öMgŻ©OHŻ®2░³╣³īŻė├Š¦ĘN║¾Ż¼ė╔ė┌ą┬╔·│╔Ą─MgŻ©OHŻ®2▒Ē├µ×ķš²ļŖ║╔Ż¼┤╦ĢrĢ■╬³ĖĮ╦«ųąĄ─OH-Ż¼▀MČ°┤┘▀MµVļxūėŠ█╝»Ż¼ūŅĮK╩╣Ą├ŲõķL┤¾▓ó├▄īŹ╗»ĪŻ
3ĪóĮYšō
ó┘ā╔╝ē┤«┬ō║╦Š¦įņ┴Ż╝╝ąg┐╔Ė▀ą¦╚ź│²╩ĶĖ╔╦«ųąĄ─Ca2+ĪóMg2+Ż¼«öę╗╝ēNaOH═Č╝ė┴┐×ķ250mg/LĪó╔Ž╔²┴„╦┘×ķ90m/hĪóŠ¦ĘNė├┴┐×ķ200kgŻ¼Č■╝ēNaOH═Č╝ė┴┐×ķ500mg/LĪó╔Ž╔²┴„╦┘×ķ40m/hĪóŠ¦ĘNė├┴┐×ķ300kgĢrŻ¼┐éė▓Č╚╚ź│²┬╩ĮėĮ³90%Ż¼ØßČ╚╚ź│²┬╩×ķ68.9%ĪŻ═¼ĢrŻ¼į┌▀B└m▀\ąąųą╚ź│²ą¦╣¹▌^ĘĆČ©ĪŻ
ó┌ĮY║ŽXRDĪóXPSĪóSEM-EDSĪóFT-IRĄ╚▒Ēš„┐╔ęį░l¼FŻ¼Ęųäeį┌Ą┌ę╗╝ē║═Ą┌Č■╝ē║╦Š¦įņ┴Żčbų├ųąą╬│╔┴╦├▄īŹĄ─CaCO3ĪóMgŻ©OHŻ®2įņ┴Ż¾wĪŻė╔ė┌æęĖĪ╬’Ą─┤µį┌Ż¼Š¦ĘN▒Ē├µĖ³╝ė┤ų▓┌Ż¼▓ó╩╣įņ┴Ż¾wFT-IR░l╔·╝tęŲŻ╗į┌▀^’¢║═Č╚Īó╦«┴”╝¶ŪąĄ─ū„ė├Ž┬Ż¼ė┌īŻė├Š¦ĘN▒Ē├µ░l╔·ĘŪŠ∙ŽÓ│╔║╦Ż¼┤┘╩╣Š¦ĘNķL┤¾ĪŻ
ó█═©▀^ZetaļŖ╬╗▒Ēš„Ż¼į┌Ė▀pHĢrŠ¦ĘN▒Ē├µŠ∙ĦžōļŖŻ¼│§Ų┌─▄ē“ėąą¦╬³ĖĮCa2+ĪóMg2+Ż¼į┌╦Ä䮥─ū„ė├Ž┬«a╔·CaCO3ĪóMgŻ©OHŻ®2▓ó╔·ķLė┌Š¦ĘN▒Ē├µŻ╗ļS║¾ė╔ė┌ą┬╔·│╔Ą─CaCO3ĪóMgŻ©OHŻ®2Ą─▒Ē├µļŖ║╔▓╗═¼Ż¼║¾└mŠ¦ĘN│ų└mķL┤¾Ą─ÖC└Ē▓╗═¼Ż¼Ą½ūŅĮKŠ∙─▄ē“╚ź│²ÅU╦«ųąĄ─Ca2+ĪóMg2+ĪŻ
ó▄ŽÓ▒╚ė┌é„ĮyĄ─╗»īW│┴ĄĒ/Ė▀├▄Č╚│┴ĄĒ│ž│²ė▓Č°čįŻ¼║╦Š¦įņ┴Ż╝╝ągŠ▀ėą╦«┴”═Ż┴¶ĢrķgČ╠Ą─ā׳cĪŻę“×ķ║╦Š¦įņ┴Żčbų├×ķžQŽ“Ż¼╣Ø╩Ī┴╦š╝Ąž├µĘeŻ╗═¼ĢrŻ¼ė╔ė┌ūŅĮK╔·│╔┴╦║¼╦«┬╩Ė³Ą═Ūę├▄īŹĄ─CaCO3ĪóMgŻ©OHŻ®2įņ┴Ż¾wŻ¼¤oąĶ║¾└m╬█─Ó╠Ä└ĒŻ¼╣Ø╩Ī┴╦š¹¾wĄ─▀\ąą┘Mė├ĪŻŻ©üĒį┤Ż║╬„░▓Į╗═©┤¾īW╚╦ŠėŁhŠ│┼cĮ©ų■╣ż│╠īWį║Ż¼ųą┐Ų║╦ØÖ<Ļā╬„>╔·æBŁhŠ│ėąŽ▐╣½╦ŠŻ¼Ļā╬„╦«äš░lš╣╝»łFėąŽ▐╣½╦ŠŻ¼ĮŁ╠Ką┬ėŅ╠ņ│╔Łh▒ŻėąŽ▐╣½╦ŠŻ®



