ŅAč§╗»╠Ä└Ē³S║ėįŁ╦«Ž¹ČŠĖ▒«a╬’╣ż╦ć▀xō±čąŠ┐
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2016-5-22 8:46:10
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį
ĪĪĪĪ³S║ė╩Ū螊Ć50ČÓū∙│Ū╩ą║═420ČÓéĆ│ŪµéĄ─╔·«aĪó╔·╗Ņė├╦«║═╔·æBė├╦«Ą─ų„ę¬╦«į┤.Į³─ĻüĒŻ¼╩▄╣ż▐rśIĪó╔·╗Ņ╬█╦«┼┼Ę┼Ą╚ė░ĒæŻ¼³S║ėėąÖC╬█╚Š╚šęµ╝ėäĪŻ¼Ė╔┴„▓┐Ęųģ^Č╬║═ų¦┴„╦«┘|ŠS│ųį┌IV~VŅÉ║═┴ėVŅÉ╦«┘|╦«ŲĮ.╩▄³S║ėüĒ╦«Ė▀─Ó╔│ė░ĒæŻ¼ę²³S╦«Äņ║═│┴╔░│ž╩Ū³S║ėŽ┬ė╬Ąžģ^Ųš▒ķ▓╔ė├Ą─š{ąŅ║═╣®╦«ĘĮ╩Į.╚╗Č°Ż¼³S║ėįŁ╦«▀M╚ļę²³S╦«Äņ╗“│┴╔░│žąŅ┤µ║¾Ż¼╦«┴„╦┘Č╚┬²Ż¼╦«Äņų▄▀ģĄ─├µį┤╬█╚Šę▓Ģ■╩╣Ą├╦«ÄņųąĄ¬┴ūĄ╚ĀIBį¬╦ž║¼┴┐į÷╝ėŻ¼ī¦ų┬įÕŅÉ┤¾┴┐Ę▒ų│╔§ų┴▒¼░l╦«╚AŻ¼╩╣Ą├ę²³S╦«Ųš▒ķ├µ┼RĖ▀ėąÖC╬’ĪóĖ▀įÕ║═Ė▀ąß╬ČĄ╚å¢Ņ}Ż¼Č°ę²³S╦«ÅS▓╔ė├Ą─│ŻęÄā¶╦«╣ż╦ćę╗░Ńļyė┌ėąą¦æ¬ī”Ż¼ę“┤╦Ż¼ī”’ŗė├╦«╦«┘|śŗ│╔┴╦ć└ųž═■├{.
ĪĪĪĪ─┐Ū░Ż¼į┌ę²³S╦«ÅS│÷╦«ųąąß╬Č║═Ž¹ČŠĖ▒«a╬’(DBPs)ØŌČ╚▌^Ė▀Ą─å¢Ņ}ė╚×ķ═╗│÷.│ŻęÄĄ─DBPsų„ę¬░³└©╚²¹u╝ū═ķ(THMs)║═¹uęę╦ß(HAAs)Ą╚.Į³─ĻüĒŻ¼ļSų°ą┬┼dÅŖĪ░╚²ų┬Ī▒╠žąįĄ─Ž¹ČŠĖ▒«a╬’ü厧░Ę(░³└©NDMA)Īó¹u┤·Ž§╗∙╝ū═ķĪó¹u┤·ęꧯ░ĘĄ╚║¼Ą¬Ž¹ČŠĖ▒«a╬’(N-DBPs)║═ĄŌ┤·Ž¹ČŠĖ▒«a╬’(I-DBPs)Ą╚ŽÓ└^▒╗░l¼FŻ¼’ŗė├╦«ųąDBPsĄ─å¢Ņ}įĮüĒįĮ╩▄ĄĮĻPūó.Ķbė┌DBPsų„ę¬Å─Ž¹ČŠä®┼c╦«ųąėąÖC╬’Ę┤æ¬ųą«a╔·Ż¼╠Į╦„╦«ųąDBPsŪ░¾w╬’ĘųūėĮM│╔ęÄ┬╔Ż¼ėąßśī”ąįĄž╠ß│÷┐žųŲĘĮĘ©Ż¼ī”ė┌ā¶╦«╣ż╦ćųąėąą¦Ž¹£pDBPs«a╔·Š▀ėą┴╝║├Ą─ųĖī¦ęŌ┴x.
ĪĪĪĪ╗»īWŅAč§╗»┐╔ĮĄĮŌ╦«ųąĄ─▓┐ĘųėąÖC╬█╚Š╬’Ż¼ÅŖ╗»│ŻęÄ╣ż╦ć╚ź│²╬█╚Š╬’Ą─ą¦╣¹Ż¼Å─Č°ŲĄĮĖ─╔Ų╦«┘|║═£p╔┘DBPs╔·│╔┴┐Ą─ū„ė├.│ŻęŖĄ─ŅAč§╗»ä®ėą┬╚(Cl2)ĪóČ■č§╗»┬╚(ClO2)ĪóĖ▀Õi╦ßŌø(KMnO4)Ą╚.蹊┐░l¼FŻ¼ė├Cl2▀MąąŅAč§╗»Ż¼─▄’@ų°ęųųŲįÕŅÉ╝░╝ÜŠ·Ą─Ę▒ų│Ż¼ĮĄĄ═╦«Ą─╔½Č╚║═╬ČĄ└Ż¼═¼Ģr─▄č§╗»▓┐ĘųDBPsĄ─Ū░¾w╬’ęįęųųŲ║¾└m╣ż╦ćųą▓┐ĘųDBPsĄ─╔·│╔.ClO2─▄č§╗»╦«ųąÄ¦ėą┴u╗∙Īó╚®╗∙ĪóĘė╗∙Ą╚║¼č§╣┘─▄łFĄ─ėąÖC┤¾Ęųūė╬’┘|Ż¼▓╗Ģ■╔·│╔┬╚┤·Ą─Ė▒«a╬’Ż¼ŪęŲõū„ė├▓╗╩▄pH║═░▒Ą─ė░Ēæ.KMnO4▓╗āH─▄ų▒Įėč§╗»╦«ųąėąÖC╬’Ż¼į┌Ę┤æ¬▀^│╠ųąą╬│╔Ą─ą┬╔·æBMnO2ę▓┐╔ęį═©▀^╬³ĖĮĪóč§╗»║═ų·─²Ą╚ū„ė├╚ź│²▓┐ĘųėąÖC╬█╚Š╬’Ż¼▓ó┤┘▀M╦«ųąŅw┴Ż╬’Ą─╣▓│┴Ż¼ėąą¦Ąž┐žųŲDBPsŪ░¾w╬’.
ĪĪĪĪę“┤╦Ż¼▒Š╬─ęį║ė─Ž╩ĪÓŹų▌╩ą╩»Ę│┴╔░│ž│┴ĄĒ║¾Ą─³S║ė╦«×ķ蹊┐ī”Ž¾Ż¼ėæšō³S║ė╦«ųąDBPsŪ░¾w╬’Ą─ĮM│╔╠žš„Ż¼ī”▒╚Ęų╬÷▓╗═¼ŅAč§╗»ä®ī”ę²³S╦«Ž¹ČŠĖ▒«a╬’╔·│╔Øō─▄Ą─ū„ė├ą¦╣¹Ż¼ęįŲ┌×ķę²³S╦«ųąėąÖC╬’ĮM│╔Ą─├„╬·║═ŅAč§╗»╣ż╦ćĄ─▀xō±╠ß╣®└Ēšō║═╝╝ągų¦│ų.
ĪĪĪĪ2 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ2.1 īŹ“×įćä®ĪóāxŲ„┼cĘų╬÷ĘĮĘ©
ĪĪĪĪįć“×╩╣ė├Ą─┴“╦ßĪóÜõč§╗»ŌcĪó┴ū╦ßČ■ÜõŌøĪó┬╚╗»õ@║═Ė▀Õi╦ßŌøĄ╚¤oÖCįć䮊∙×ķā×╝ē║═Ęų╬÷╝āįć䮯¼Š∙┘Åūįć°╦Ä╝»łF╗»īWįćä®ėąŽ▐╣½╦Š(╔Ž║Ż).╝ū╗∙╩ÕČĪ╗∙├č(MTBE)Īóš²╬ņ═ķĪó╝ū┤╝║═ęęļµĄ╚×ķ╔½ūV╝āįć䮯¼┘ÅūįJ.T.Baker(USA).╚▄ĮŌąįėąÖC╠╝(DOC)Ą─ś╦£╩śėŲĘŠ∙┘Å┘Iūįć°╝ęŁh▒Ż▓┐ś╦£╩śėŲĘ蹊┐╦∙.┤╬┬╚╦ßŌc(ėąą¦┬╚ØŌČ╚52 g Īż L-1Ż¼ęįCl2ėŗ)×ķā×╝ē╝āįć䮯¼┘Åūįė┌├└ć°Sigma-Aldrich╣½╦Š.┼õų├īŹ“×╦∙ėą╚▄ę║Ą─│¼╝ā╦«üĒūįMilli-Q╝ā╦«ÖC(Referenceą═Ż¼├└ć°Millpore╣½╦Š).Ž¹ČŠĖ▒«a╬’ś╦£╩śėŲĘ╚²¹u╝ū═ķ(THMs)┼c║¼Ą¬Ž¹ČŠĖ▒«a╬’(N-DBPs)╗ņś╦Š∙┘Åūįė┌├└ć°Sigma-Aldrich╣½╦Š.įć“×ųą╩╣ė├Ą─ClO2(ØŌČ╚×ķ0.3%)▓╔ė├TwinOxideżq(De TongelreepŻ¼Netherl and s)Ą─įćä®A(5 güå┬╚╦ßŌc║═╠Ē╝ėä®)║═įćä®B(5 gę╗╦«║Ž┴“╦ßÜõŌc║═╠Ē╝ėä®)Ž╚║¾╝ė╚ļ250 mL│¼╝ā╦«ųąĮø╗ņ║ŽČ°│╔.
ĪĪĪĪīŹ“×╦∙ė├įŁ╦«╚Īūį║ė─Ž╩ĪÓŹų▌╩ą╩»ĘįŁ╦«ÅSŻ¼Ųõų„ę¬╦«┘|ųĖś╦╚ń▒Ē 1╦∙╩Š.pH£yČ©▓╔ė├FE20-FiveEasyŠ½├▄pHėŗ(Mettler ToledoŻ¼╚╩┐);UV254£yČ©▓╔ė├UNICO 4802ūŽ═Ō┐╔ęŖĘų╣Ō╣ŌČ╚ėŗ.╦«śė┬╚╗»Ž¹ČŠĖ▒«a╬’╔·│╔Øō─▄┼ÓBįć“׊∙ć└Ė±┐ž£žį┌25 ĪµŚl╝■Ž┬▀Mąą.Ž¹ČŠĖ▒«a╬’╚²¹u╝ū═ķ(THMs)Īó¹uęęļµ(HANs)╝░╚²┬╚Ž§╗∙╝ū═ķ(TCNM)Ą╚ō]░ląį DBPsŠ∙▓╔ė├GC-ECDĘĮĘ©Ęų╬÷Ż¼╩╣ė├āxŲ„×ķŹuĮ“GC2010.įć“×Ęų╬÷ųą▓╔ė├HP5├½╝Ü╣▄ų∙(30 mĪ┴0.25 mmŻ¼0.25 ”╠mŻ¼J&W)ū„×ķĘųļxų∙.
▒Ē1 ³S║ėįŁ╦«╦«┘|ųĖś╦
ĪĪĪĪ2.2 īŹ“×ĘĮĘ© 2.2.1 įŁ╦«ųąDOMĘųūė┴┐Ęų▓╝īŹ“×
ĪĪĪĪīŹ“×▓╔ė├│¼×V─żĘ©(UF)£yČ©╦«ųą╚▄ĮŌąįėąÖC╬’(DOM)║═Ž¹ČŠĖ▒«a╬’Ū░¾w╬’Ęųūė┴┐Ą─Ęų▓╝╠žąį.įŁ╦«Įø0.45 ”╠m×V─ż▀^×V║¾Ż¼ė╔Ė▀╝āĄ¬ÜŌ(99.999%)╠ß╣®0.15 MPaū¾ėęĄ─▀^─żē║┴”Ż¼Ęųäe═©▀^ŪąĖŅĘųūė┴┐×ķ30Īó10Īó5║═1 kDaĄ─UF─żŻ¼└¹ė├▓Ņ£pĘ©Ą├ĄĮ5ĮM║¼ėą▓╗═¼Ęųūė┴┐DOMĄ─įŁ╦«Ż¼▓ó£yČ©─ż║¾╦«Ą─Ė„ĒŚ╦«┘|ųĖś╦Ż¼░³└©┐é╚▄ĮŌąįėąÖC╠╝(DOC)ĪóUV254ĪóŽ¹ČŠĖ▒«a╬’╔·│╔Øō─▄(DBPFP).Ęųūė┴┐Ęųļxįć“×▀^│╠ųąŻ¼│ų└m└¹ė├┤┼┴”öć░Ķčbų├öć░ĶęįĘ└ų╣ØŌ▓ŅśO╗»ī”įć“×ĮY╣¹«a╔·ė░Ēæ. 2.2.2 įŁ╦«ųąDOMėH╩Ķ╦«ąįĘųļxīŹ“× īŹ“×▓╔ė├AmberliteXAD-8║═XAD-4śõų¼┤«┬ō▀MąąDOMėH╩Ķ╦«ąįĘųļxŻ¼▀^ų∙ų«Ū░Ž╚ė├5 mol Īż L-1 HClīóįć“×╦«śėpHš{ų┴2.0Ż¼īóXAD-8┼cXAD-4ā╔ų╗╠Ņ│õų∙┤«┬ōŻ¼ų├ė┌╣╠ŽÓ▌═╚Īčbų├╔ŽŻ¼═©▀^Ė¶─ż▒├šµ┐š│ķ╬³Ż¼╦«śėę└┤╬═©▀^ā╔ų¦śõų¼ų∙.╬³ĖĮį┌XAD-8śõų¼Ą─DOM×ķÅŖ╩Ķ╦«ąįėąÖC╬’Ż¼╬³ĖĮį┌XAD-4śõų¼Ą─DOM╩Ū╚§╩Ķ╦«ąįėąÖC╬’Ż¼Č°═©▀^ā╔ĘNśõų¼ų∙║¾Ą─DOMät×ķėH╦«ąįėąÖC╬’.ā╔ų¦śõų¼ų∙╔ŽĄ─ėąÖC╬’Ęųäe▓╔ė├0.1 mol Īż L-1 NaOH▀MąąŽ┤├ōŻ¼╝ė╦ß╗žš{ų┴ųąąįęįéõ║¾└mįć“×£yČ©;Įø▀^ā╔ų¦śõų¼ų∙║¾Ą─▀^×Vę║ė├╚▌Ų„│ąĮėŻ¼ąĶ╝ėēA╗žš{ų┴ųąąį║¾▀Mąą║¾└mįć“×.▓╔ė├śõų¼ĘųļxDOMąĶ▀Mąą╗ž╩š┬╩Ęų╬÷Ż¼ęįUV254ĪóDOCėŗŻ¼ŲõėąÖC╬’╗ž╩š┬╩į┌80%~120%ų«ķg.
ĪĪĪĪ2.2.3 ╦«śėŅAč§╗»ĘĮĘ©┼cģóöĄ
ĪĪĪĪĖ∙ō■3ĘN▓╗═¼Ą─ŅAč§╗»ä®┤╬┬╚╦ßŌc(ęįCl2ėŗ)ĪóČ■č§╗»┬╚(ClO2)║═Ė▀Õi╦ßŌø(KMnO4)Ż¼īóīŹ“×Ęų×ķ3ĮM.├┐ĮMŠ∙╚Ī1.2 LįŁ╦«čb╚ļ6éĆ┤¾¤²▒ŁųąŻ¼▓ó░┤šš0~5▀MąąŠÄ╠¢Ż¼▓óęį80 r Īż min-1Ą─▐D╦┘öć░Ķ30 min.öć░Ķķ_╩╝║¾Ż¼┴ó╝┤╝ė╚ļ═¼ĘNĄ─▓╗═¼═Č╝ė┴┐Ą─ŅAč§╗»ä®.Ė∙ō■╦«ÅSĄ─╦«┴┐╝░▓╗═¼č§╗»ä®Ą─ąį─▄▓Ņ«ÉŻ¼├┐ĮM╝ė╚ļ▓╗═¼ä®┴┐Ą─ŅAč§╗»ä®Ż¼6Ę▌╦«śėųąCl2║═ClO2═Č╝ė┴┐Š∙Ęųäe×ķ0(┐š░ūśė)Īó0.5Īó1.0Īó1.5Īó2.0║═3.0 mg Īż L-1(ŅAč§╗»ä®═Č╝ė┴┐ŠÄ╠¢0~5)Ż¼KMnO4Ą─═Č╝ė┴┐Ęųäe×ķ0(┐š░ūśė)Īó0.1Īó0.2Īó0.4Īó0.6║═0.8 mg Īż L-1(ŅAč§╗»ä®═Č╝ė┴┐ŠÄ╠¢0~5).ŅAč§╗»öć░ĶĮY╩°║¾Ż¼╚Ī0.2 L╦«śė£yįć╦«┘|Ą─DBPsŻ¼═¼Ģrīó╦«śė▀^0.45 ”╠mĄ─×V─ż║¾▀MąąDBPFPĄ─┼ÓB£yįć. 2.2.4 Ž¹ČŠĖ▒«a╬’╔·│╔Øō─▄(DBPFP)£yįć ╦«śėĮø▀^0.45 ”╠m┤ū╦ß└wŠS─ż▀^×V║¾Ż¼╚Ī50 mLĘ┼╚ļŽ┤ā¶Ą─¤²▒ŁŻ¼╝ė┬╚Ū░ś╦Č©ØŌČ╚Ż¼╝ė┬╚┴┐Ė∙ō■Ė„╦«śėĄ─╦«┘|ģóöĄųĄŻ¼░┤╬─½I╣½╩Įėŗ╦Ń.▀xė├┴ū╦ß¹}ŠÅø_¾wŽĄ(10 mmol Īż L-1)Ż¼└¹ė├╦ßēAš{╣Ø╚▄ę║pHųĄ×ķ7.00Ī└0.02.īóęį╔Ž╦«śėčbØM45 mL░▓┼ÓŲ┐Ż¼▓ó╩╣ė├ĦėąŠ█╦─Ę·ęꎮē|Ų¼Ą─╔wūė╔wŠoŻ¼£yįćŲ┐Ę┤æ¬▀^│╠ąĶ▒ŻūC¤oÜŌ┼▌.╦«śėĘ┼ų├ė┌║┌░ĄŁhŠ│Ą─┼ÓBŽõā╚Ż¼£žČ╚┐žųŲ×ķ(25Ī└1)Īµ.ę╗░Ń7 d║¾╔·│╔Øō─▄Ę┤æ¬ĮY╩°Ż¼Ž“┼ÓBę║ųą╝ė╚ļ▀^┴┐Na2SO3╗“NH4Clīó╩ŻėÓ┬╚┤Ń£ńŻ¼▒M┐ņ▌═╚Ī║¾▀MąąĘų╬÷.
ĪĪĪĪ3 ĮY╣¹┼cėæšō
ĪĪĪĪ3.1 įŁ╦«ųąDOMĘųūėĘų▓╝ĮM│╔ęÄ┬╔
ĪĪĪĪ3.1.1 įŁ╦«ųąDOM┼cDBPFPĄ─Ęųūė┴┐Ęų▓╝╠žąį
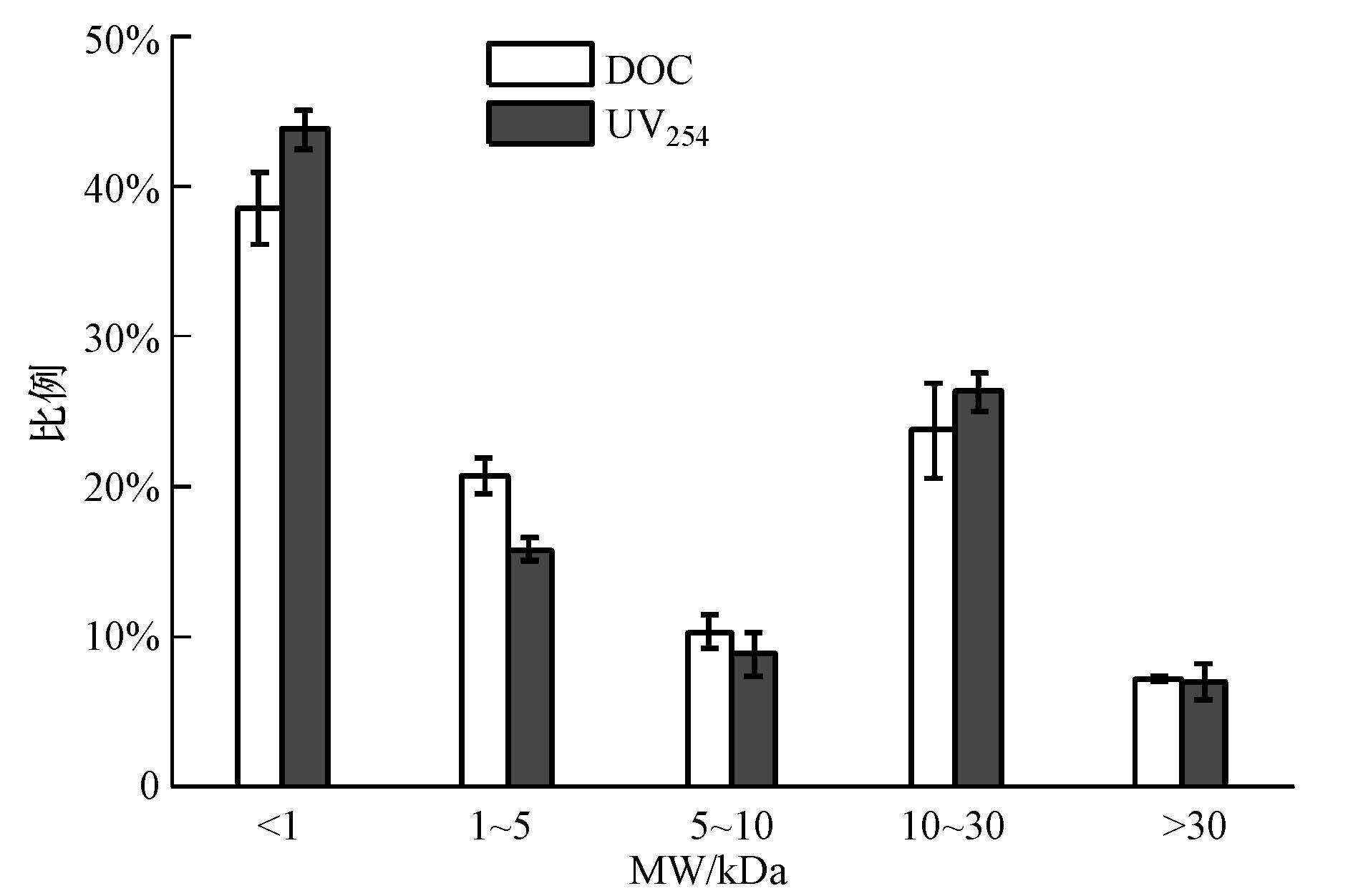
ĪĪĪĪæ¬ė├▓╗═¼Įž┴¶Ęųūė┴┐Ą─UF─żī”³S║ėįŁ╦«ųąDOM▀MąąĘųļx║¾Ż¼Ė„śėŲĘĘųäe£yČ©DOCĪóUV254║═DBPsŪ░¾w╬’Ą─║¼┴┐Ż¼Įøėŗ╦ŃĖ„Ęųūėģ^ķgDOC║¼┴┐║═UV254╚ńłD 1╦∙╩ŠŻ¼THMs║═N-DBPs╔·│╔Øō─▄Ęų▓╝╚ńłD 2╦∙╩Š.
łD1 ³S║ėįŁ╦«ųąDOMĄ─Ęųūė┴┐Ęų▓╝
ĪĪĪĪÅ─łD 1┐╔ęį┐┤│÷Ż¼³S║ėįŁ╦«Ą─DOC║¼┴┐Ė∙ō■Ęųūė┴┐(MW)╣▓Ęų×ķ5ĮM(<1 kDaĪó1~5 kDaĪó5~10 kDaĪó10~30 kDaĪó>30 kDa)Ż¼Ųõš╝┐é┴┐Ą─░┘Ęų▒╚ę└┤╬×ķ38.39%Īó20.59%Īó10.23%Īó23.65%║═7.14%Ż¼Ė„Ęųūė┴┐ģ^ķgā╚UV254Ą─Ęų▓╝ęÄ┬╔┼cDOCŽÓę╗ų┬Ż¼▒╚└²Ęųäe×ķ43.96%Īó15.52%Īó7.76%Īó25.01%║═7.81%.ŲõųąŻ¼MW <1 kDaĮMĘųĄ─▒╚└²ūŅĖ▀Ż¼MW <5 kDaĮMĘųĄ─DOC╝sš╝┐é┴┐Ą─60%.Ęų╬÷ĮY╣¹▒Ē├„Ż¼³S║ėįŁ╦«ųąDOMų„ę¬ęįąĪĘųūė┴┐┤µį┌ą╬╩Į×ķų„.
ĪĪĪĪÅ─łD 2┐╔ęįŪÕ│■Ąž┐┤│÷Ż¼³S║ėįŁ╦«Įø▀^┬╚╗»DBPsØō─▄┼ÓB║¾Ż¼┐╔Öz£yĄĮ4ĘN╚²¹u╝ū═ķ(THMs)Ż¼Ęųäe×ķ┬╚Ę┬(CF)ĪóČ■┬╚ę╗õÕ╝ū═ķ(BDCM)Īóę╗┬╚Č■õÕ╝ū═ķ(DBCM)║═╚²õÕ╝ū═ķ(BF);▀Ć─▄Öz£yĄĮ╚²┬╚Ž§╗∙╝ū═ķ(TCNM)ĪóČ■┬╚ęęļµ(DCAN)Īó╚²┬╚ęęļµ(TCAN)Īóę╗┬╚ę╗õÕęęļµ(BCAN)║═Č■õÕęęļµ(DBAN)Ą╚5ĘN║¼Ą¬Ž¹ČŠĖ▒«a╬’(N-DBPs).³S║ėįŁ╦«ųąĖ„Ęųūėģ^ķgėąÖC╬’Įø┬╚╗»║¾Č╝ėąTHMs║═N-DBPs╔·│╔Ż¼ŲõųąŻ¼MW <1 kDaĮMĘųŠ▀ėąūŅĖ▀Ą─THMs║═N-DBPs╔·│╔Øō─▄.▀@ę╗ĮY╣¹šf├„MW<1 kDaĄ─ĮMĘų╩Ū╔·│╔DBPsĄ─ų„ę¬Ū░¾w╬’Ż¼▀@┼cGangĄ╚ī”▓╗═¼Ęųūė┴┐Ą─Ū░¾w╬’ī”ė┌╚²¹u╝ū═ķ╔·│╔Øō─▄ė░ĒæĄ─蹊┐ĮY╣¹ŽÓ╦Ų.ę╗░ŃČ°čįŻ¼ąĪĘųūė┴┐Ą─DOM ČÓ║¼ėąĘ╝ŽŃ▒ĮŁh║═¶╚╗∙Ż¼Ė³ęū╔·│╔THMs;Č°ąĪĘųūė┴┐DOMųąĄ─░▒╗∙╦ßĪóÓč▀╩║═ÓūÓżĄ╚║¼Ą¬ėąÖC╬’(DON)ät╩ŪHANsĄ─ų„ę¬Ū░¾w╬’.ę“┤╦Ż¼─▄▌^║├ĄžĮŌßī³S║ėįŁ╦«ųąMW<1 kDaĄ─ėąÖC╬’ĮMĘųDBPFP┼ÓB║¾╔·│╔Ą─THMs║═N-DBPs┴┐ūŅ┤¾.Ė∙ō■ŽÓĻP蹊┐Ż¼į┌║¾└mĄ─╦«╠Ä└Ē╣ż╦ćųą▓╔ė├╔·╬’╗Ņąį╠┐╬³ĖĮĪó╣Ō┤▀╗»č§╗»Īó─ż╝╝ągĄ╚Š∙ī”ąĪĘųūė┴┐ėąÖC╬’Ą─╚ź│²ėą║▄║├Ą─ą¦╣¹.
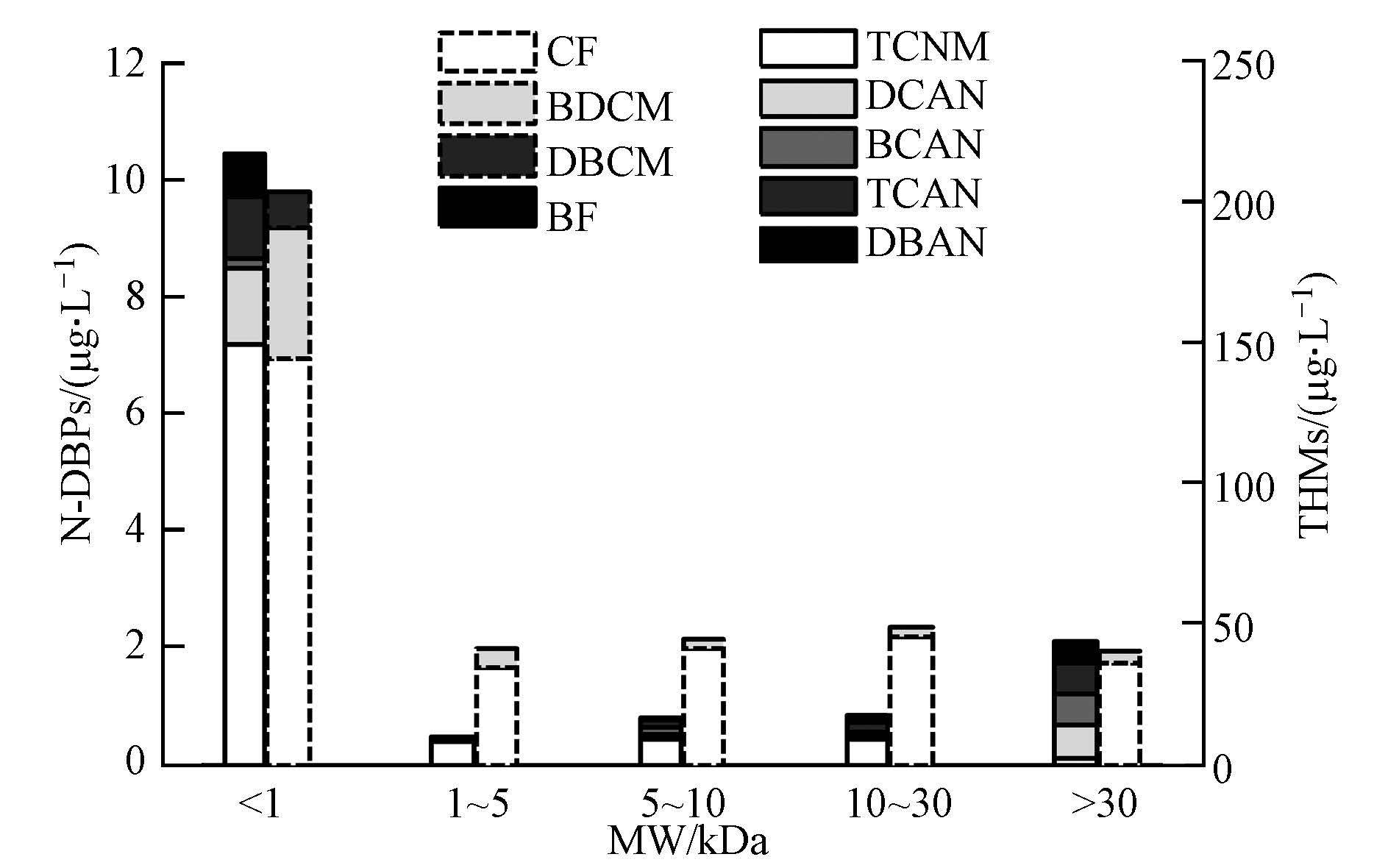
łD2 įŁ╦«ųąĖ„ŅÉą═DBPs╔·│╔Øō─▄Ęųūė┴┐Ęų▓╝
ĪĪĪĪ3.1.2 įŁ╦«ųąDOM┼cDBPFPĄ─ėH╩Ķ╦«ąįĘų▓╝╠žąį
ĪĪĪĪ├■ŪÕįŁ╦«ųąėąÖC╬’Ą─ėH╩Ķ╦«╠žąįĘų▓╝ęÄ┬╔ī”ė┌ėąßśī”ąį▀xō±╦«╠Ä└Ē╣ż╦ćŠ▀ėą▌^ÅŖĄ─ųĖī¦ęŌ┴x.×ķ┤╦Ż¼▒Š╬─▓╔ė├śõų¼ĘųļxĘ©½@Ą├┴╦³S║ėįŁ╦«ųąDOM┼cDBPsŪ░¾w╬’Ą─ėH╩Ķ╦«Ęų▓╝╠žąįŻ¼ŲõĮY╣¹Ęųäe╚ńłD 3║═4╦∙╩Š.
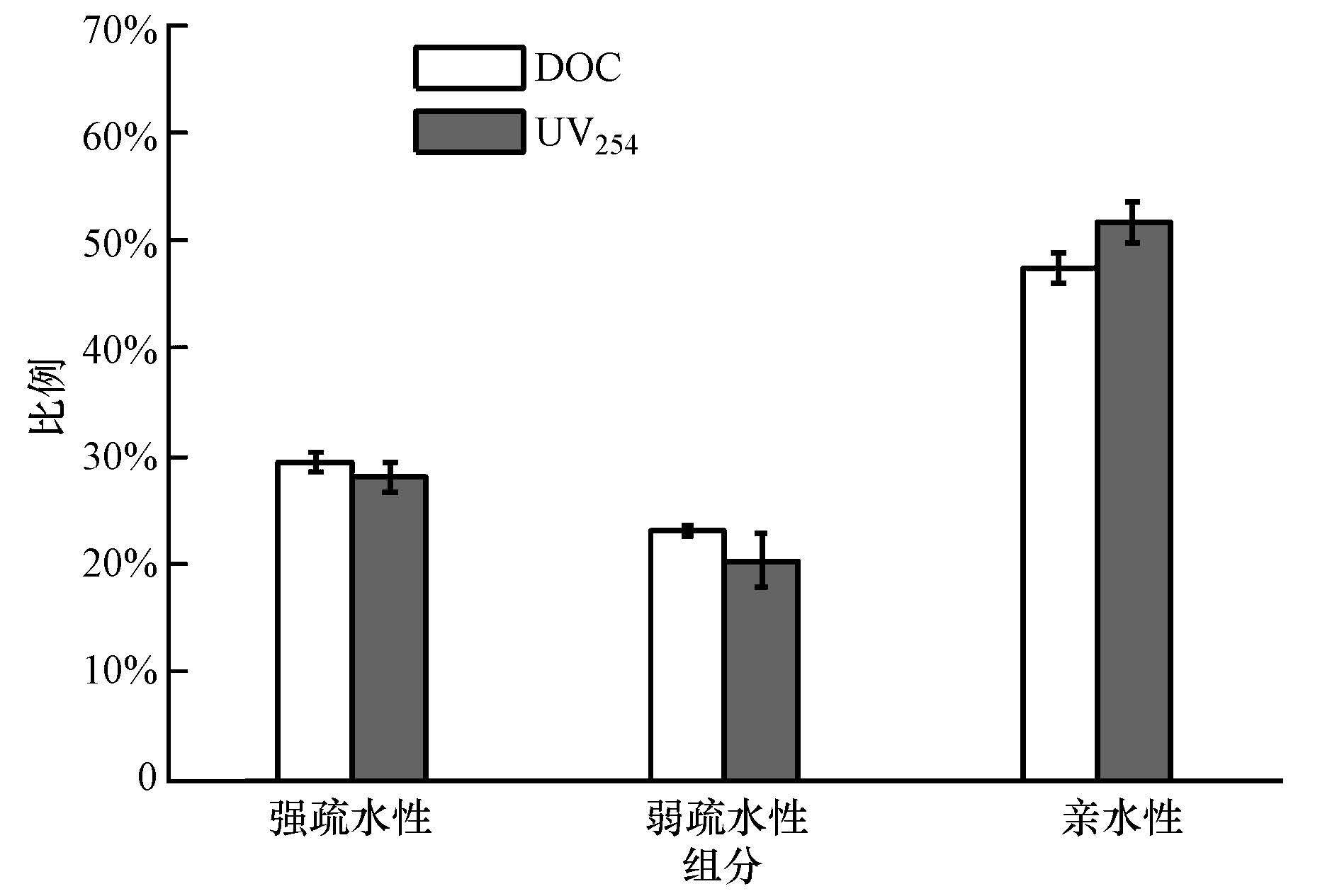
łD3 ³S║ėįŁ╦«ųąDOMĄ─ėH╩Ķ╦«Ęų▓╝╠žąį
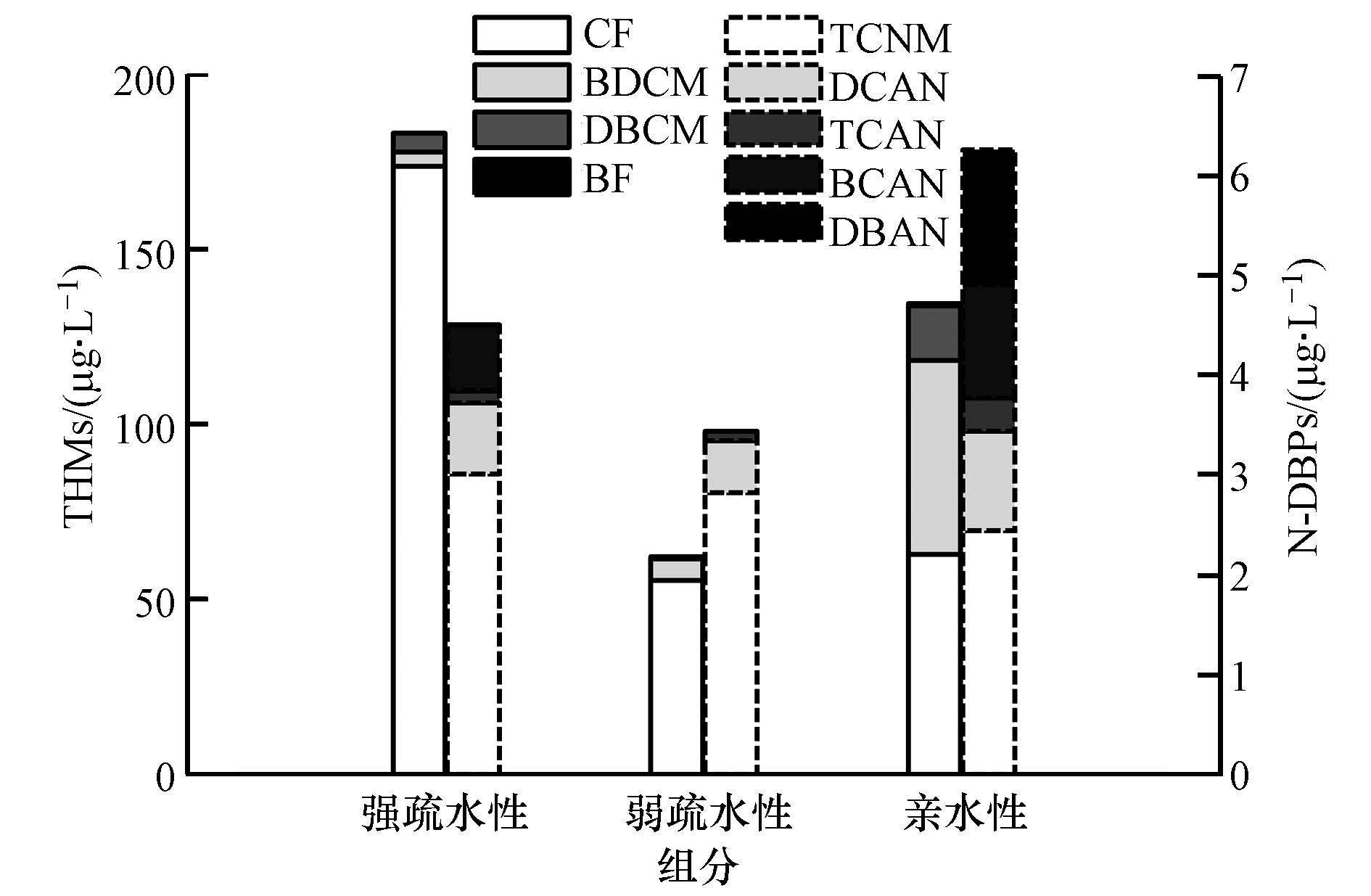
łD4 Ė„ėH╩Ķ╦«ąįĮMĘųĄ─DBPs╔·│╔Øō─▄
ĪĪĪĪÅ─łD 3ųą┐╔ęį┐┤│÷Ż¼«ö³S║ėįŁ╦«ųąĖ„ėH╩Ķ╦«ąįėąÖC╬’Ą─ĮM│╔╠žąįė├DOC▒Ēš„ĢrŻ¼Å─Ė▀ĄĮĄ═ę└┤╬×ķėH╦«ąįĮMĘųĪóÅŖ╩Ķ╦«ąįĮMĘų║═╚§╩Ķ╦«ąįĮMĘųŻ¼Ųõ║¼┴┐░┘Ęų▒╚Ęųäe×ķ47.49%Īó29.43%║═23.08%;«öė├UV254▒Ēš„ĢrŻ¼Ęųäe×ķ50.00%Īó30.84%║═19.16%.┐é¾w╔ŽČ°čįŻ¼³S║ėįŁ╦«ųąĄ─DOM╩Ūęį╩Ķ╦«ąįĮMĘų┤µį┌ą╬╩Į×ķų„Ż¼įōĮY╣¹ę▓▒Ē├„³S║ėįŁ╦«ųą║¼ėą▌^ČÓĄ─Ė»ų│╦ß║═Ė╗└’╦ߥ╚ŅÉą═╬’┘|.
ĪĪĪĪłD 4×ķ³S║ėįŁ╦«ųąĖ„ėH╩Ķ╦«ąįĮMĘųĄ─DBPs╔·│╔Øō─▄.░┤THMs╔·│╔┴┐Å─Ė▀ĄĮĄ═ę└┤╬×ķŻ║ÅŖ╩Ķ╦«ąįĮMĘų>ėH╦«ąįĮMĘų>╚§╩Ķ╦«ąįĮMĘųŻ¼ŽÓæ¬Ą─ØŌČ╚Ęųäe×ķ173.00Īó146.81║═55.40 ”╠g Īż L-1.ė╔ė┌įŁ╦«ųąĄ─Br-į┌XADśõų¼╔ŽŠ∙▓╗▒Ż┴¶Ż¼ę“┤╦Ż¼ÅŖ╩Ķ╦«ąį║═╚§╩Ķ╦«ąįĮMĘų▓ó╬┤╔·│╔õÕ┤·THMs.Č°ėH╦«ąįėąÖC╬’Ą─ų¼ĘŠūÕ╗»║Ž╬’į┌┬╚╗»┼ÓBųąęū┼cBr-Ę┤æ¬╔·│╔║¼õÕĄ─THMsŻ¼ę“┤╦Ż¼į┌ėH╦«ąįĮMĘųųąÖz£yĄĮ┴╦▓┐ĘųõÕ┤·THMs.ī”▒╚łD 3ųąDOC║═UV254öĄō■▓╗ļy░l¼FŻ¼ļm╚╗ÅŖ╩Ķ╦«ąįĮMĘųį┌³S║ė╦«ųą╦∙š╝▒╚└²×ķĄ┌2╬╗Ż¼Ą½Ųõ╔·│╔THMsĄ─┴┐ūŅĖ▀(łD 4).┐é¾wČ°čįŻ¼╩Ķ╦«ąįĮMĘųĄ─THMs╔·│╔Øō─▄┤¾ė┌ėH╦«ąįĮMĘųŻ¼▀@╩Ūę“×ķ╩Ķ╦«ąįėąÖC╬’║¼ėąŽÓī”▌^ČÓĄ─Ę╝ŽŃŅÉ╬’┘|Ż¼ęū╔·│╔THMs.į┌║¾└mĄ─╠Ä└ĒųąŻ¼▓╔ė├╗ņ─²Ą╚╣ż╦ćī”╩Ķ╦«ąįĮMĘųŠ▀ėą▌^║├Ą─╚ź│²ą¦╣¹.░┤N-DBPs╔·│╔┴┐Å─Ė▀ĄĮĄ═ę└┤╬×ķŻ║ėH╦«ąįĮMĘų>ÅŖ╩Ķ╦«ąįĮMĘų>╚§╩Ķ╦«ąįĮMĘų.ŲõųąŻ¼ėH╦«ąįĮMĘųŠ▀ėąūŅ┤¾Ą─N-DBPs╔·│╔Øō─▄Ż¼ØŌČ╚×ķ6.91 ”╠g Īż L-1Ż¼╝sš╝┐é┴┐Ą─50%.▓╗ļy░l¼FŻ¼³S║ėįŁ╦«ųąĄ─ėH╦«ąįĮMĘų╩ŪN-DBPsĄ─ų„ę¬üĒį┤Ż¼▀@ę▓┼c╦«ųą╚▄ĮŌąįėąÖCĄ¬(DON)ų„ę¬ė╔░▒╗∙╦ߥ╚ėH╦«ąį╬’┘|ĮM│╔Ą─╠žąį╩ŪŽÓę╗ų┬Ą─.
ĪĪĪĪ3.2 ▓╗═¼╗»īWŅAč§╗»ĘĮĘ©ī”įŁ╦«ųąDOM╠Ä└Ēą¦╣¹ī”▒╚
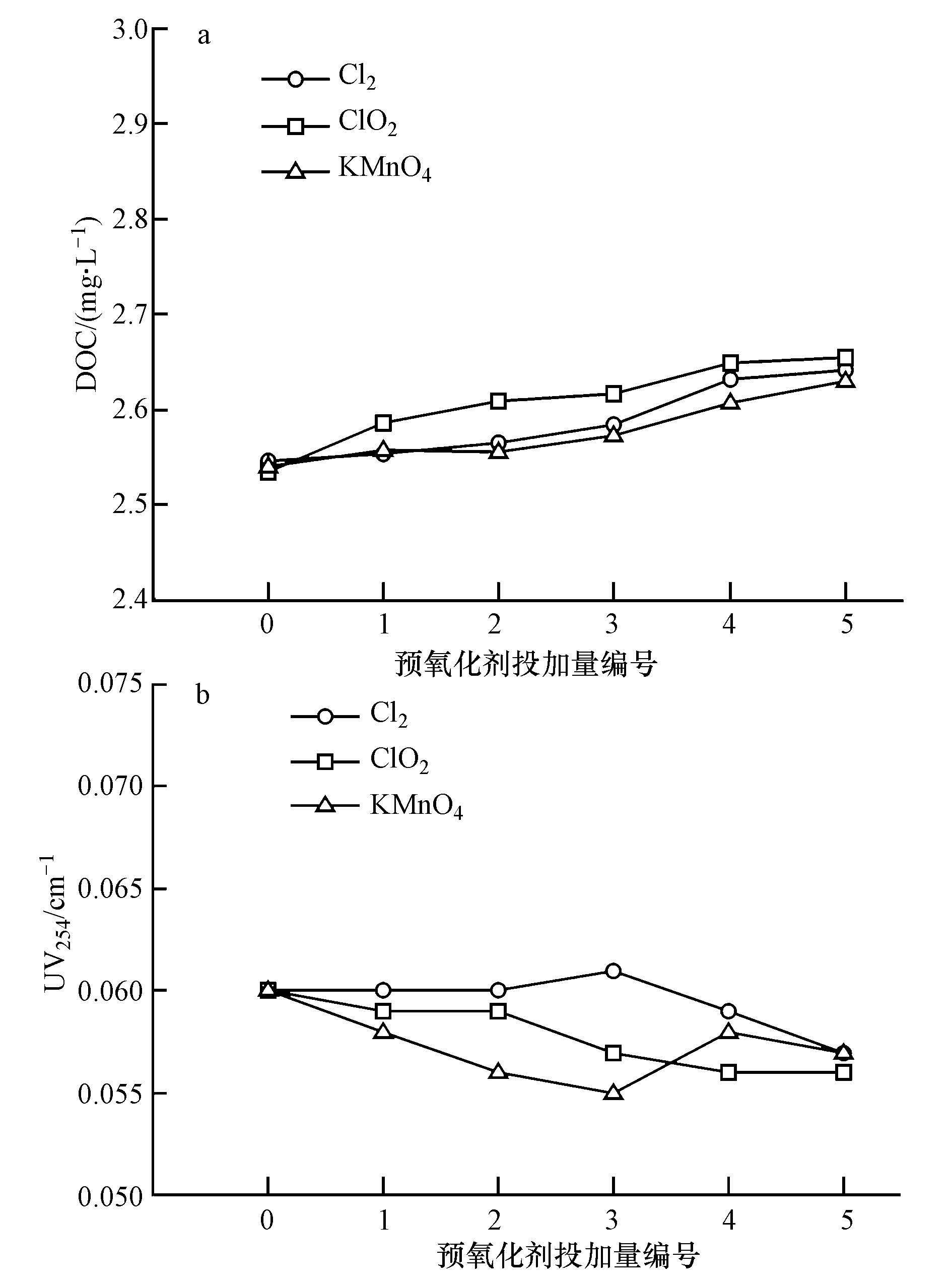
ĪĪĪĪ▓╔ė├NaClOĪóClO2║═KMnO4 3ĘNŅAč§╗»ä®Ż¼į┌▓╗═¼═Č╝ė┴┐Ž┬╠Ä└Ē³S║ėįŁ╦«╦«śėŻ¼Įø│õĘųĘ┤æ¬║¾Ė„╦«śėDOC║═UV254Ą─ūā╗»╚ńłD 5╦∙╩Š.
łD5 ▓╗═¼ŅAč§╗»ä®═Č╝ė┴┐Ž┬³S║ėįŁ╦«Ą─DOC(a)║═UV254(b)ūā╗»
ĪĪĪĪÅ─łD 5a┐╔ęį┐┤│÷Ż¼Įø╗»īWŅAč§╗»ū„ė├║¾Ż¼³S║ėįŁ╦«Ą─DOCŠ∙│÷¼F┴╦ąĪĘ∙Č╚╔Ž╔².«öClO2║═Cl2═Č╝ė┴┐Č╝×ķ3 mg Īż L-1ĢrŻ¼DOCĘųäeį÷ķL┴╦4.74%║═3.73%Ż¼ClO2╠Ä└ĒĄ─ØqĘ∙▌^▒╚ŅA┬╚╗»┤¾.▀@┐╔─▄╩Ūę“×ķClO2Ą─č§╗»─▄┴”╩ŪCl2Ą─2.6▒ČŻ¼─▄ėąą¦č§╗»╦«ųą┤µį┌Ą─įÕĄ╚╔·╬’╝Ü░¹ā╚Ą─├ĖŻ¼┐ņ╦┘┐žųŲ╔·╬’Ą░░ū┘|Ą─║Ž│╔Ż¼╩╣─żĄ─ØB═Ėąįį÷Ė▀Ż¼Å─Č°ī¦ų┬╝Ü░¹ßīĘ┼ā╚▓┐ėąÖC┘|Ż¼ę“┤╦Ż¼ĮøClO2ū„ė├║¾Ą─╦«śėDOC╔Ž╔²├„’@.KMnO4┐╔┤╠╝żįÕŅÉ▀^Č╚Ęų├┌░¹ā╚╬’┘|Ż¼╗“═©▀^ŲõÅŖč§╗»ąįŲŲē─╝Ü░¹▒┌Ż¼įņ│╔░¹ā╚╬’┘|═Ō┴„Ż¼╝┤▒Ē¼F×ķĮøKMnO4ŅAč§╗»ū„ė├║¾Ą─╦«śėDOCę▓│÷¼Fę╗Č©╔Ž╔².Ą½ĮøKMnO4ŅAč§╗»║¾³S║ėįŁ╦«DOC╔Ž╔²Ę∙Č╚▌^ąĪŻ¼▀@┐╔─▄╩Ūę“×ķKMnO4Ą─č§╗»─▄┴”▌^╚§Ż¼═¼ĢrŲõ▀ĆįŁ«a╬’MnO2═©▀^╬³ĖĮū„ė├ķgĮėĄ─╚ź│²┴╦ę╗▓┐ĘųėąÖC╬’Ż¼▓ó┤┘▀M╦«ųąŅw┴Ż╬’Ą─╣▓│┴╦∙ų┬.
ĪĪĪĪ┼cDOCĄ─ūā╗»▓╗═¼Ż¼Įø▓╗═¼ŅAč§╗»ä®ū„ė├║¾Ż¼³S║ėįŁ╦«Ą─UV254ųØu£pąĪ(łD 5b)Ż¼▀@▒Ē╩Š╦«ųąĄ─Ę╝ŽŃūÕėąÖC╬’╗“─│ą®Š▀ėą╣▓▄ŚļpµIĄ─ėąÖC╬’į┌╦«ųąĄ├ĄĮ┴╦ę╗Č©Ą─╚ź│².ŲõųąŻ¼ClO2į┌═Č╝ė┴┐▌^ąĪĢrŻ¼UV254ø]ėąūā╗»Ż¼ļSų°Ųõ═Č╝ė┴┐Ą─į÷╝ėŻ¼UV254Ž┬ĮĄ┌ģä▌├„’@.▀@┐╔─▄╩Ūė╔ė┌ClO2═Č╝ė┴┐┤¾ĢrŻ¼Ųõč§╗»ąįĄ├ĄĮ┴╦╝ėÅŖ.Č°KMnO4į┌ū„×ķŅAč§╗»ä®ĢrŻ¼UV254│╩¼FŽ╚Ž┬ĮĄ║¾╔Ž╔²Ą─┌ģä▌Ż¼┐╔─▄╩ŪKMnO4į┌č§╗»Ę╝ŽŃūÕėąÖC╬’╗“Š▀ėą╣▓▄ŚļpµIĄ─ėąÖC╬’Ą─═¼ĢrŻ¼č§╗»ĘųĮŌ┴╦─│ą®┤¾ĘųūėėąÖC╬’Ż¼ėų╔·│╔┴╦Š▀ėąŅÉ╦ŲĮYśŗĄ─ėąÖC╬’.Ą½Įø▀^Cl2ŅAč§╗»║¾Ż¼UV254ø]ėą’@ų°Ą─ūā╗»Ż¼▀@┐╔─▄╩Ūė╔ė┌Cl2Ą─č§╗»─▄┴”▒╚ClO2┼cKMnO4╚§Ż¼ī”╦«ųąĘ╝ŽŃūÕėąÖC╬’Ą─╚ź│²ą¦╣¹ŽÓī”▌^▓Ņ╦∙ī¦ų┬.
ĪĪĪĪ3.3 ▓╗═¼ŅAč§╗»ĘĮĘ©Ž¹£p³S║ėįŁ╦«ųąŽ¹ČŠĖ▒«a╬’╔·│╔Øō─▄Ą─ī”▒╚Ęų╬÷
ĪĪĪĪ3.3.1 ╗»īWŅAč§╗»▀^│╠ųąDBPsų▒Įė╔·│╔
ĪĪĪĪĮøClO2║═KMnO4ŅAč§╗»║¾Ż¼³S║ėįŁ╦«ųąTHMs╔·│╔┴┐ø]ėąį÷╝ėŻ¼ų╗Öz£yĄĮ³S║ė╦«ųąįŁ▒Š║¼ėąĄ─╚²┬╚╝ū═ķ(CF)Ż¼ØŌČ╚╝s×ķ4.30 ”╠g Īż L-1Ż¼═¼Ģrę▓╬┤Öz£y│÷N-DBPs.▀@╩Ūę“×ķClO2║═KMnO4╗∙▒Š▓╗┼c╦«ųąDOM░l╔·¹u╗»ū„ė├.ĮøCl2ŅAč§╗»║¾Ż¼³S║ėįŁ╦«ųą╔·│╔Ą─DBPsĖ┼ør╚ńłD 6╦∙╩Š.
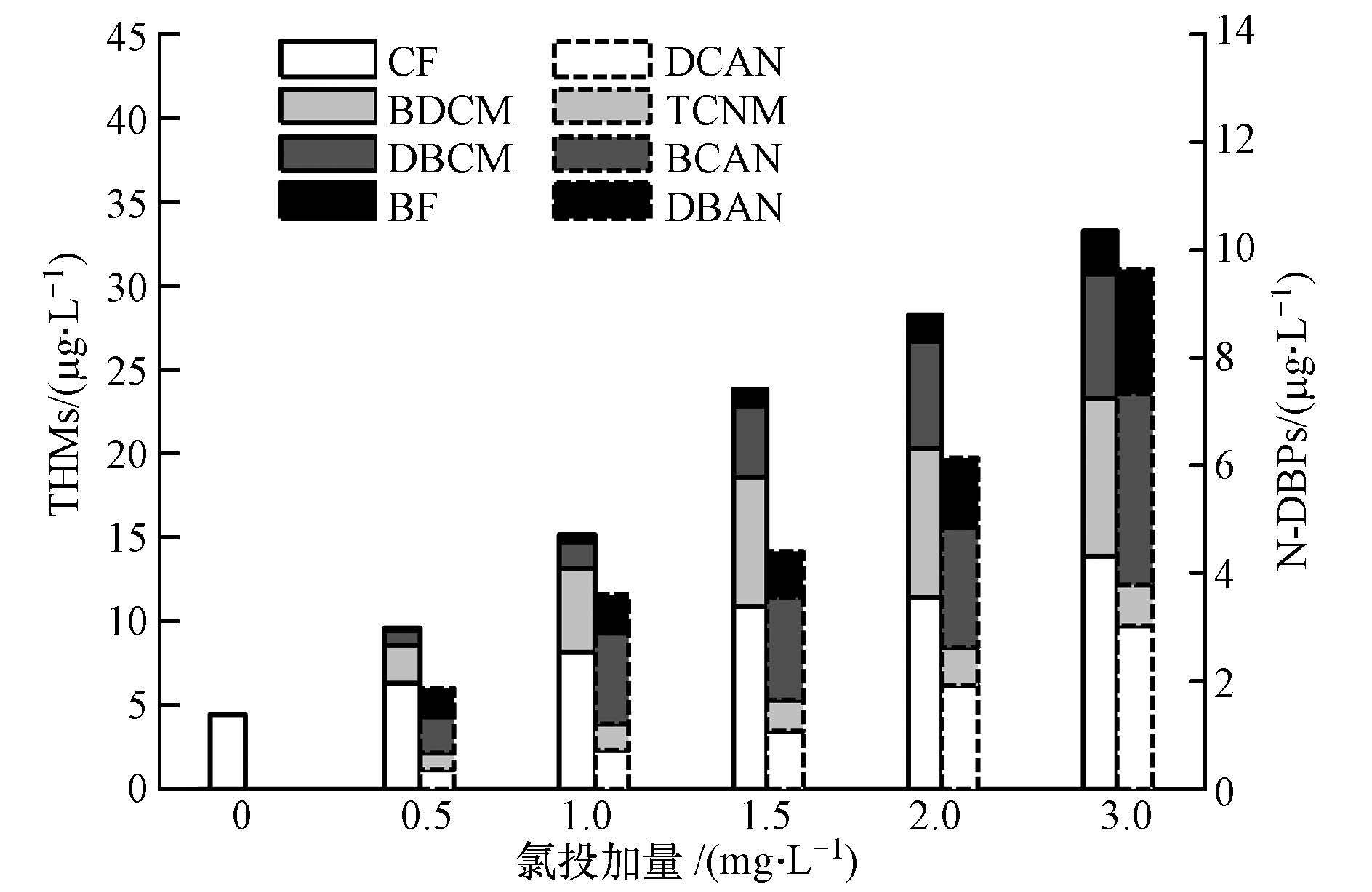
łD6 ▓╗═¼═Č╝ė┴┐Cl2ŅAč§╗»³S║ėįŁ╦«ųą╔·│╔Ą─DBPs
ĪĪĪĪÅ─łD 6ųą┐╔ęį┐┤│÷Ż¼ĮøCl2ŅAč§╗»║¾Ż¼³S║ėįŁ╦«ųąĄ─DBPsļSų°┬╚═Č╝ė┴┐Ą─į÷╝ėČ°ę└┤╬į÷╝ė.▀@ų„ę¬╩Ūę“×ķ³S║ėįŁ╦«ųą┤µį┌┤¾┴┐ęū┼cCl2░l╔·Ę┤æ¬Ą─ėąÖC╬’Ż¼╩╣Ą├ļSų°Cl2═Č╝ė┴┐Ą─į÷╝ėŻ¼THMs║═N-DBPs╔·│╔┴┐╝▒äĪ╔Ž╔².ļSų°╝ė┬╚┴┐Ą─į÷╝ėŻ¼į┌╔·│╔Ą─THMs║═¹uęęļµ(HANs)ųąŻ¼õÕ┤·Ą─THMs║═HANs(BCNA║═DBAN)╝s×ķ┐éHANsĄ─40%~60%Ż¼▀@┼cįŁ╦«ųą║¼ėą▌^Ė▀ØŌČ╚Ą─Br-(0.06 mg Īż L-1)ėąĻP.į┌Cl2ŅAč§╗»▀^│╠ųąŻ¼Br-─▄┼c┤╬┬╚╦ßą╬│╔č§╗»ąįĖ³ÅŖĄ─┤╬õÕ╦ß(HOBr)Ż¼▓ó┼cįŁ╦«ųąĄ─ėąÖC╬’░l╔·č§╗»Īó╚Ī┤·║═╝ė│╔Ą╚╗»īWĘ┤æ¬Ż¼╔·│╔┤¾┴┐õÕ┤·DBPs.ė╔ė┌õÕ┤·DBPsĄ─Ī░╚²ų┬Ī▒╠žąį▀hĖ▀ė┌┬╚┤·DBPsŻ¼ę“┤╦Ż¼³S║ėįŁ╦«æ¬ė├ŅA┬╚╗»╣ż╦ćĢræ¬ųž³cĻPūóŲõ«a╔·Ą─’LļU.
ĪĪĪĪ3.3.2 ╗»īWŅAč§╗»╣ż╦ćī”DBPs╔·│╔Øō─▄Ą─╠Ä└Ēą¦╣¹ī”▒╚
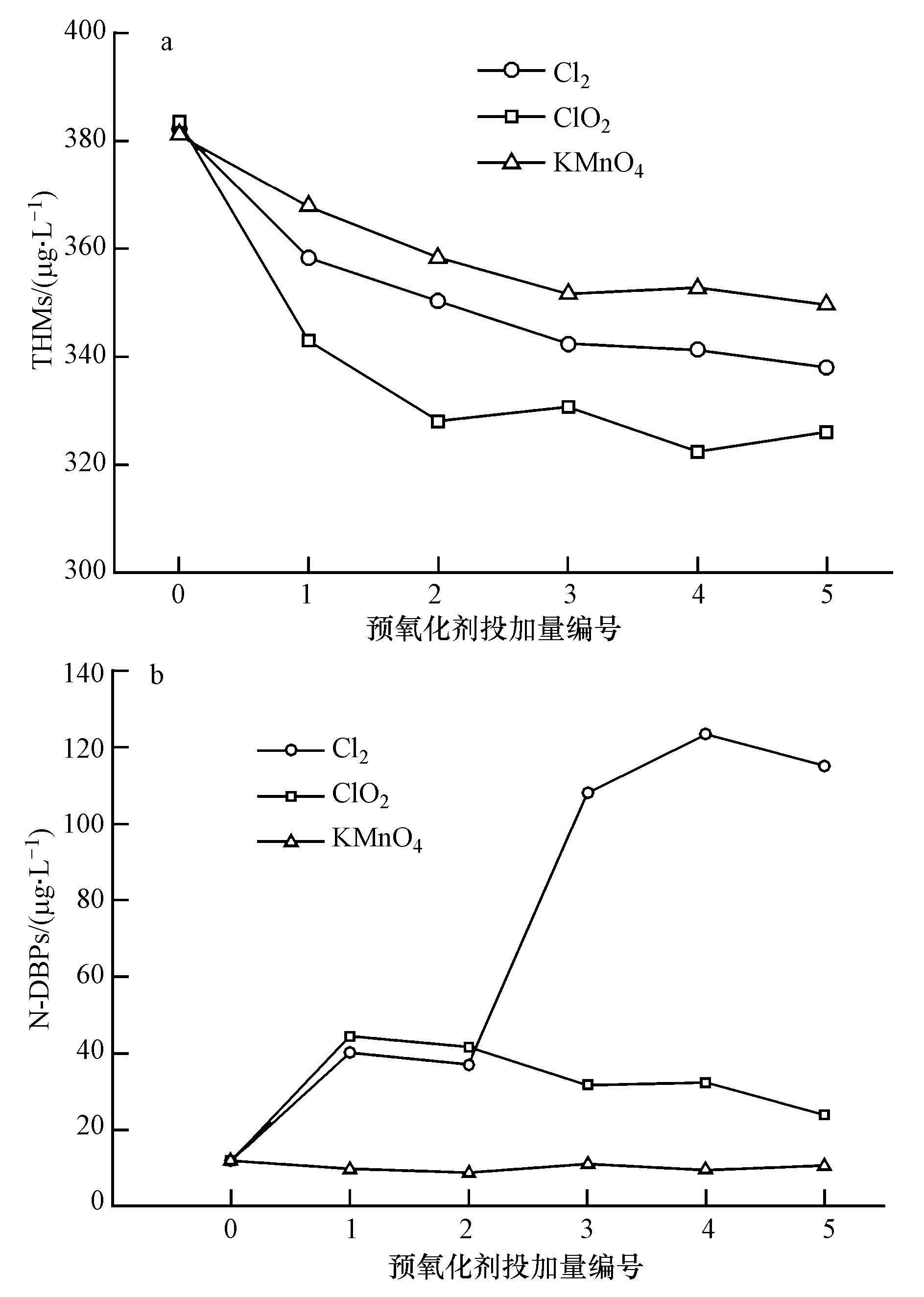
ĪĪĪĪĶbė┌╗»īWŅAč§╗»ä®Š∙Š▀ėą▌^ÅŖĄ─č§╗»─▄┴”Ż¼╝ė╚ļ╦«ųąŠ∙┐╔┼c╦«ųą┤µį┌Ą─DOM░l╔·Ę┤æ¬Ż¼Ė─ūāįŁėąĄ─DOM╗»īWĮYśŗŻ¼Å─Č°ė░ĒæĄĮā¶╦«╣ż╦ćųą║¾└mŽ¹ČŠ▀^│╠ųąDBPs«a╔·╠žąį.×ķ┤╦Ż¼▒Š╬─蹊┐┴╦Cl2ĪóClO2║═KMnO4č§╗»║¾Ė„ŅÉą═DBPs╔·│╔Øō─▄ūā╗»Ą─ęÄ┬╔Ż¼ļS═Č╝ė┴┐ūā╗»THMs║═N-DBPs╔·│╔Øō─▄ūā╗»╚ńłD 7╦∙╩Š.
łD7 ▓╗═¼ŅAč§╗»ä®║══Č╝ė┴┐Ž┬³S║ėįŁ╦«Ą─THMs(a)║═N-DBPs(b)╔·│╔Øō─▄ūā╗»
ĪĪĪĪė╔łD 7a┐╔ęįŪÕ│■Ąž┐┤│÷Ż¼3ĘNŅAč§╗»ä®Š∙┐╔ęįį┌ę╗Č©│╠Č╚Ž¹£pTHMs╔·│╔Øō─▄Ż¼ŲõųąŻ¼ClO2ŅAč§╗»ą¦╣¹├„’@║├ė┌KMnO4ŅAč§╗»║═Cl2ŅAč§╗».═¼ĢrŻ¼ļSų°ŅAč§╗»ä®═Č╝ė┴┐Ą─ų▓Įį÷╝ė³S║ėįŁ╦«THMFP│╩¼Fķ_╩╝┐ņ╦┘Ž┬ĮĄ║¾ų▓Į┌ģė┌ĘĆČ©Ą─┌ģä▌.«öClO2ĪóCl2║═KMnO4═Č╝ė┴┐Ęųäe×ķ1.0Īó1.0║═0.8 mg Īż L-1ĢrŻ¼³S║ėįŁ╦«Ą─THMFPĮĄĄ═░┘Ęų▒╚Ęųäe×ķ14.47%Īó8.39%║═8.25%.▓╗ļy┐┤│÷Ż¼3ĘNŅAč§╗»ä®ī”³S║ėįŁ╦«Ą─THMFPĄ─Ž„£pą¦╣¹ę└┤╬×ķClO2>Cl2>KMnO4.3ĘNŅAč§╗»ä®Š∙┐╔ęį═©▀^č§╗»ū„ė├Ė─ūā╦«ųąėąÖC╬’Ą─ĮYśŗŻ¼ėąą¦ĮĄĄ═THMsŪ░¾w╬’║¼┴┐Ż¼╩╣ų«▌^ļy┼c║¾└mŽ¹ČŠ▀^│╠ųąŅA┬╚░l╔·Ę┤æ¬╔·│╔THMs.ą¦╣¹ūŅ║├Ą─ClO2č§╗»─▄┴”ūŅÅŖŻ¼┐╔īó═¬Īó§źĪó¶╚╦ßĪó╚®ĪóĘėĄ╚╬’┘|č§╗»×ķ┤╝Īó░ĘĪó├čĪó═ķ¤NŅÉėąÖC╬’Ż¼īóÅ═ļsĄ─Ę╝ŽŃŅÉėąÖC╬’č§╗»ĘųĮŌ×ķ║åå╬Ą─║¼č§µ£ĀŅėąÖC╬’Ż¼╩╣ėąÖC╬’č§ķ_ŁhĪóöÓµ£.
ĪĪĪĪÅ─łD 7b┐╔ęį┐┤│÷Ż¼╗»īWŅAč§╗»╗∙▒Š▓╗ī”³S║ėįŁ╦«N-DBPs╔·│╔Øō─▄«a╔·Ž¹£pŻ¼Cl2║═ClO2ŅAč§╗»║¾N-DBPs╔·│╔Øō─▄┤¾┤¾į÷╝ėŻ¼ė╚Ųõ╩Ū▌^Ė▀═Č╝ė┴┐Ą─Cl2ŅAč§╗»▀^│╠.«öCl2ŅAč§╗»ĢrŻ¼N-DBPFPļSų°Cl2═Č╝ė┴┐Ą─į÷╝ė▓╗öÓ╔Ž╔²Ż¼ŲõųąŻ¼╔·│╔Ą─N-DBPs┤¾▓┐Ęų×ķHANs.«öCl2═Č╝ė┴┐×ķ2.00 mg Īż L-1ĢrŻ¼N-DBPFP▀_ĄĮ┴╦ūŅ┤¾ųĄ123.40 ”╠g Īż L-1Ż¼HANs║═TCNM╔·│╔Øō─▄Ęųäeš╝ĄĮ┴╦┐é┴┐Ą─92.03%║═7.97%.Ęų╬÷ŲõįŁę“╩ŪŻ¼³S║ėįŁ╦«ųą┤µį┌Ą─įÕŅÉĄ╚ėąÖC╬’ĮøCl2ŅAč§╗»║¾Ż¼┐╔╔·│╔▌^ČÓĄ─HANsŪ░¾w╬’Ż¼Č°▀@ą®Ū░¾w╬’ėųļyė┌į┌▌^Č╠Ģrķgā╚▒╗┬╚▀Mę╗▓ĮĘųĮŌŻ¼ę“┤╦Ż¼N-DBPs╔·│╔Øō─▄┤¾Ę∙Č╚į÷╝ė.ClO2į┌═Č╝ė┴┐▌^ąĪĢrŻ¼N-DBPFPėą╦∙╔Ž╔²Ż¼ų«║¾ļSų°ClO2Ą─═Č╝ė┴┐▓╗öÓį÷╝ėŻ¼ClO2Ą─č§╗»ū„ė├╝ėÅŖŻ¼č§╗»┴╦▓┐ĘųN-DBPsŪ░¾w╬’Ż¼╩╣Ą├N-DBPFP£p╔┘.KMnO4Ą─═Č╝ė┴┐ī”N-DBPFPø]ėą├„’@Ą─ė░ĒæŻ¼▀@┐╔─▄┼cKMnO4▀xō±ąįč§╗»╠žąįėąĻPŻ¼▀@┼cĻÉųę┴ųĄ╚ī”ė┌Ė▀Õi╦ßŌø┐žųŲ¹uęę╦ß╔·│╔Ą─蹊┐ę╗ų┬.┐é¾wČ°čįŻ¼ŅAč§╗»ä®Ą─═Č╝ė▓╗─▄ėąą¦Ąž£p╔┘N-DBPFPŻ¼3ĘNŅAč§╗»ä®┐žųŲN-DBPFPĄ─ą¦╣¹ę└┤╬×ķŻ║KMnO4>ClO2>Cl2.×ķ┴╦ėąą¦Ąž┐žųŲN-DBPsĄ─╔·│╔Ż¼Į©ūh▓╔ė├╔·╬’Įėė|č§╗»Ę©ĪóĘ█─®╗Ņąį╠┐╬³ĖĮ╣ż╦ćĄ╚ī”N-DBPsŪ░¾w╬’▀Mąą▀Mę╗▓ĮĄ─╚ź│².
ĪĪĪĪŠC║Ž┐╝æ]THMs║═N-DBPs┐éĄ─╔·│╔Øō─▄Ż¼«öClO2║═KMnO4Ą─═Č╝ė┴┐Č╝×ķ3 mg Īż L-1ĢrŻ¼DBPs╔·│╔┴┐Ą─╚ź│²┬╩Ęųäe▀_ĄĮ┴╦11.21%║═8.63%.Ą½╩╣ė├Cl2ŅAč§╗»ĢrĘ┤Č°╩╣DBPsĄ─╔·│╔┴┐į÷╝ė┴╦14.97%Ż¼▀@┼c╠’Ė╗ŽõĄ╚ė├▓╗═¼ŅAč§╗»ĘĮĘ©ī”ė┌³SŲųĮŁįŁ╦«┬╚(░Ę)╗»ė░ĒæĄ─蹊┐ę╗ų┬Ż¼ę“┤╦Ż¼³S║ė╦«ų▒ĮėŅA┬╚╗»Ą─░▓╚½ąįųĄĄ├ĻPūó.ŠC║Ž┐╝æ]ŅAč§╗»Ą─ą¦─▄Ż¼ęį╝░ī”║¾└mŽ¹ČŠĖ▒«a╬’Ą─ė░ĒæŻ¼į┌īŹļH╣ż╦ć▀^│╠ųąæ¬▒▄├ŌĖ▀═Č┴┐Ą─ŅA┬╚╗»╣ż╦ćŻ¼╦«ÅSŚl╝■▀\ąąĄ─įÆŻ¼┐╔ā׎╚▓╔ė├ClO2║═KMnO4ū„×ķŅAč§╗»ä®╠Ä└Ē╬ó╬█╚Š³S║ėįŁ╦«.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.bnynw.comĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
ĪĪĪĪ4 ĮY šō
ĪĪĪĪ1)³S║ėįŁ╦«ųąDOMų„ę¬ęįąĪĘųūėą╬╩Į┤µį┌Ż¼ŪęMW <1 kDaĄ─ĮMĘų╩Ū╔·│╔DBPsĄ─ų„ę¬Ū░¾w╬’.³S║ėįŁ╦«ęį╩Ķ╦«ąįĮMĘų×ķų„Ż¼ŲõųąŻ¼╩Ķ╦«ąįėąÖC╬’╩Ū╔·│╔THMsĄ─ų„ę¬Ū░¾w╬’Ż¼ėH╦«ąįėąÖC╬’╩Ū╔·│╔N-DBPsĄ─ų„ę¬Ū░¾w╬’.
ĪĪĪĪ2)ĮøClO2║═KMnO4ŅAč§╗»Ą─³S║ėįŁ╦«DBPsø]ėąį÷╝ėŻ¼ĮøCl2ŅAč§╗»║¾Ą─³S║ėįŁ╦«DBPs╔·│╔┴┐ļSų°Cl2═Č╝ė┴┐į÷╝ėČ°ųØuį÷╝ė.3ĘNŅAč§╗»ä®ĮĄĄ═³S║ėįŁ╦«THMFPĄ─ą¦╣¹×ķClO2>Cl2>KMnO4Ż¼Ą½3ĘNŅAč§╗»ä®Š∙▓╗─▄ėąą¦Ąž£p╔┘N-DBPFP.
ĪĪĪĪ3)į┌īŹļH╣ż╦ć▀^│╠ųąŻ¼╦«ÅSæ¬▒M┴┐▒▄├ŌĖ▀═Č┴┐Ą─ŅA┬╚╗»╣ż╦ćŻ¼┐╔ā׎╚▓╔ė├ClO2╗“KMnO4ū„×ķŅAč§╗»ä®╠Ä└Ē╬ó╬█╚Š³S║ėįŁ╦«.