Ė▀╝ēč§╗»╣ż╦ć(advancedoxidationprocesses,AOPs)═©▀^«a╔·ÅŖč§╗»ąįĄ─┴u╗∙ūįė╔╗∙(ĪżOH)Īó╗Ņąį┬╚ūįė╔╗∙(RCSŻ¼░³└©ClĪżĪóClOĪżĄ╚)║═│¼č§ūįė╔╗∙(O2Īż-)Ą╚┐╔ī”╦«¾wųą╦Ä╬’┼céĆ╚╦ūo└ĒŲĘ(pharmaceuticalsandpersonalcareproducts,PPCPs)ŅÉ╬█╚Š╬’▀Mąąėąą¦╚ź│²ĪŻ
╗∙ė┌NaClOĄ─AOPsęč▒╗ÅVĘ║ĄžčąŠ┐▓óæ¬ė├ė┌īŹ█`ĪŻūŽ═Ō/┤╬┬╚╦ßŌc(UV/NaClO)╣ż╦ćī”╬█╚Š╬’ėąĖ▀ą¦Ą─╚ź│²─▄┴”Ż¼═¼Ģrį┌ųąąįĪó╦ßąįŚl╝■Ž┬ī”╬█╚Š╬’Ą─ĮĄĮŌą¦╣¹Ė▀ė┌Ųõ╦¹AOPsĪŻ╚╗Č°Ż¼ėąčąŠ┐▒Ē├„Ż¼╗∙ė┌NaClOĄ─AOPsė╔ė┌┬╚Ą─ę²╚ļ┐╔─▄«a╔·ČÓĘNŠ▀ėąĪ░╚²ų┬Ī▒ū„ė├Ą─Ž¹ČŠĖ▒«a╬’(disinfectionby-products,DBPs)Ż¼╚ń║╬┤_▒ŻĖ▀ą¦╚ź│²╬█╚Š╬’═¼ĢrĮĄĄ═DBPsĄ─╔·│╔│╔×ķ┴╦«öŪ░UV/NaClO╣ż╦ćĄ─蹊┐¤ß³cĪŻĮ³─ĻüĒŻ¼▀^╠╝╦ßŌc(SPC)ę“ŽÓ▌^ė┌ę║æBH2O2Š▀ėą▒Ńė┌▀\▌öĪóārĖ±▒Ńę╦Ą─ā׳cęč▒╗æ¬ė├ė┌╦«╠Ä└ĒųąĪŻ╗∙ė┌ūŽ═ŌĄ─ūŽ═Ō/▀^╠╝╦ßŌc(UV/SPC)╣ż╦ć─▄«a╔·ĪżOHĪóO2Īż-║═╠╝╦ßĖ∙ūįė╔╗∙(CO3Īż-)Ż¼┐╔ėąą¦╚ź│²╬█╚Š╬’ĪŻ
─┐Ū░ĻPė┌é„ĮyĄ─UV/NaClO║═ą┬┼dĄ─UV/SPC╣ż╦ćå╬¬ÜĮĄĮŌPPCPsĄ─蹊┐ėąįSČÓł¾Ą└Ż¼Ą½ī”2ĘN╣ż╦ćĮĄĮŌPPCPsĄ─ī”▒╚蹊┐ł¾Ą└▌^╔┘Ż¼ĮĄĮŌ▀^│╠ųą2ĘN╣ż╦ćĄ─ą¦─▄▓Ņ«ÉąĶę¬▀Mę╗▓Į蹊┐ĪŻ╦«ŚŅ╦ß(salicylicacid,SA)╩Ūę╗ĘNĄõą═Ą─PPCPŻ¼ę╗ĒŚßśī”ÅVų▌Ąž▒Ē╝░ĄžŽ┬╦«Ą─PPCPsš{▓ķ▒Ē├„SA┤µį┌ė┌╦∙ėąš{▓ķ╦«śėųąŻ¼Ųõ┘|┴┐ØŌČ╚ūŅĖ▀▀_ĄĮ2014.4”╠gĪżL−1ĪŻ▒Š╬─ęįSA×ķ─┐ś╦╬’Ż¼ī”▒╚┐╝▓ņ┴╦UV/NaClO║═UV/SPC2ĘN╣ż╦ćī”SAĄ─╚ź│²Ż¼ę²╚ļģf═¼ę“ūė(R)Ż¼┐╝▓ņ┴╦č§╗»ä®═Č╝ė┴┐ĪópHĪóĻÄļxūė(NO3−ĪóHCO3−)║═Ė»ų│╦ß(HA)Ą╚ę“╦žī”SA╚ź│²Ą─ė░ĒæŻ¼═©▀^Ęų╬÷SAĄ─├▄Č╚Ę║║»└Ēšō(DFT)ŪęĮY║ŽLC-MS┼cGC-MSĄ─ĶbČ©«a╬’Ż¼▀Mę╗▓ĮĘų╬÷┐╔─▄Ą─ĮĄĮŌ┬ĘÅĮŻ¼▓╔ė├ECOSAR│╠ą“ī”«a╬’▀Mąą┴╦ČŠąį─ŻöMŻ¼ęįŲ┌×ķ╚ź│²╦«ųąPPCPsĄ─▓╗═¼╣ż╦ć▀xō±╠ß╣®ģó┐╝ĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 ▓─┴Ž┼cāxŲ„
╦«ŚŅ╦ß(SAŻ¼╝āČ╚ŻŠ99.9%Ż¼Ą┬ć°Dr.Ehrenstorfer)Ż╗▀^╠╝╦ßŌc(SPCŻ¼CP)Ż╗╬Õ╦«┴“┤·┴“╦ßŌc(Na2S2O3Īż5H2O2Ż¼AR)Īóęęļµ(C2H3NŻ¼HPLC)Ą╚┘Åė┌░▓ūVīŹ“×┐Ų╝╝╣╔Ę▌ėąŽ▐╣½╦ŠĪŻNaClOĪóH2O2ĪóNaOHĪóHClĪóNaHCO3ĪóCH3COOHĪóHAĄ╚┘Åė┌ć°╦Ä╝»łF╗»īWįćä®ėąŽ▐╣½╦ŠŻ¼│²NaClO×ķ╗»īW╝ā═ŌŲõėÓŠ∙×ķĘų╬÷╝āĪŻīŹ“×ė├╦«×ķMilli-Q│¼╝ā╦«ĪŻ
Ė▀ą¦ę║ŽÓ╔½ūVāx(HPLC)(LC-20AŻ¼╚š▒ŠŹuĮ“)Īóę║ŽÓ╔½ūV┘|ūV┬ōė├āxLC-MS(LCMS-1200Ż¼░▓Į▌éÉ┐Ų╝╝ėąŽ▐╣½╦Š)ĪóÜŌŽÓ╔½ūV┘|ūV┬ōė├āx(GCMS-QP2010Ż¼╚š▒ŠŹuĮ“)Īó┐éėąÖC╠╝Ęų╬÷āx(TOC-VCPHŻ¼╚š▒ŠŹuĮ“)Īó▒Ńöy╩ĮėÓ┬╚ėŗ(CL200Ż¼╔Ž║Ż╚²ą┼āx▒ĒÅS)ĪópHėŗ(ST2100Ż¼│Żų▌ŖW║└╦╣āxŲ„ėąŽ▐╣½╦Š)Īó┤┼┴”öć░ĶŲ„(HJ-6AŻ¼ĮŁ╠KĮē»ŹśÄVāxŲ„)Īó╝ā╦«ÖC(Milli-QŻ¼├└ć°Milipore)ĪŻ
1.2 īŹ“×ĘĮĘ©
į┌1éĆ╚▌Ęe×ķ500mLĄ─łAų∙ą╬╚▌Ų„ųą▀MąąīŹ“ׯ¼╚▌Ų„ų├ė┌┤┼┴”öć░ĶŲ„╔ŽĪŻ╣Ōį┤×ķ╠ūėą╩»ėó╠ū╣▄Ą─Ą═ē║╣»¤¶(▌Ś╔õššČ╚0.18mW·cm−2Ż¼▓©ķL254nm)ĪŻīŹ“×╚▄ę║×ķ300mL500”╠g·L−1Ą─SA╚▄ę║Ż¼īŹ“×Ū░ė├0.1mol·L−1Ą─NaOH╗“HClīóŲõš{╣ØpHų┴7ĪŻīŹ“×ķ_╩╝Ģr═Č╝ėę╗Č©ØŌČ╚Ą─NaClO╗“SPCŻ¼═¼Ģrķ_åó╣»¤¶┼c┤┼┴”öć░ĶŲ„Ż¼ķ_╩╝ėŗĢrŻ¼į┌įOČ©Ģrķg╚ĪśėĮø0.22”╠m×V─ż▀^─ż║¾╦═╚ļHPLCĘų╬÷ĪŻ▀MśėŲ┐į┌īŹ“×ķ_╩╝Ū░ŅAŽ╚╝ė╚ļ10”╠LØŌČ╚×ķ0.01mol·L−1Ą─Na2S2O3Īż5H2O2ęį┤_▒Ż═Ļ╚½┤Ń£ń╩ŻėÓč§╗»ä®ĪŻį┌ŅAīŹ“×ųąŻ¼NaClO┼cSPCĄ─═Č╝ė┴┐Ęųäe×ķ3mg·L−1║═12mg·L−1Ģr2ĘN╣ż╦ćĄ├ĄĮ▌^║├╚ź│²ą¦╣¹Ż¼╣╩║¾└mīŹ“×ęį┤╦═Č╝ė┴┐×ķ╗∙ĄA▀MąąĪŻ╦∙ėąīŹ“×ųžÅ═3┤╬▓ó╚ĪŲĮŠ∙ųĄĪŻ
1.3 Ęų╬÷ĘĮĘ©
SAĄ─ØŌČ╚▓╔ė├HPLC▀MąąÖz£yĪŻ┴„äėŽÓA×ķ0.1%ęę╦ß╚▄ę║Ż¼┴„äėŽÓB×ķęęļµŻ¼A┼cB¾wĘe▒╚×ķ65:35Ż¼┴„╦┘×ķ1mL·min−1Ż¼ūŽ═ŌÖz£yŲ„▓©ķL×ķ292nmŻ¼ų∙£ž×ķ40ĪµŻ¼▀Mśė¾wĘe20”╠LĪŻ
1.4 «a╬’ĶbČ©ĘĮĘ©
SAĄ─ĮĄĮŌ«a╬’▓╔ė├GC-MS║═LC-MS▀MąąÖz£yĪŻŲõųąGC-MSĘų╬÷Ū░śėŲĘąĶĮøĖ╗╝»║═ŅA╠Ä└ĒĪŻīóĘ┤æ¬╚▄ę║ęį1mL·min−1Ą─┴„╦┘═©▀^╣╠ŽÓ▌═╚ĪąĪų∙Ż¼═Ļ│╔╠Ņ┴ŽĄ─Ė╗╝»║¾ė├10mLĄ─╝ū┤╝ęį0.5mL·min−1Ą─┴„╦┘▀MąąŽ┤├ōŻ¼═Ļ│╔Ž┤├ō║¾▀MśėĪŻ
GC-MSŚl╝■Ż║▀Mśė┴┐1”╠LŻ¼ļxūėį┤£žČ╚230ĪµŻ¼▀Mśė┐┌£žČ╚280ĪµŻ¼╚▄ä®Ūą│²Ģrķg4minŻ¼ķōųĄ1000Ż╗╚½Æ▀├Ķ─Ż╩ĮŻ¼Æ▀├ĶķgĖ¶0.3sŻ¼Öz£yĘČć·×ķ35~450ĪŻLC-MSŚl╝■Ż║▓╔ė├žōļxūė─Ż╩ĮŻ¼▀Mśė┴┐10”╠LŻ¼┴„äėŽÓA×ķ10%ęęļµŻ¼┴„äėŽÓB×ķ90%ØŌČ╚×ķ0.1%Ą─ęę╦ß╚▄ę║Ż¼Ą╚Č╚Ž┤├ōŻ¼┴„╦┘×ķ1mL·L−1Ż¼ų∙£ž40ĪµŻ¼Ūą│²╚▄ä®3minŻ¼į┤£žČ╚100ĪµŻ¼╚½Æ▀├Ķ─Ż╩ĮŻ¼Æ▀├ĶķgĖ¶0.3sŻ¼┘|║╔▒╚(m/z)×ķ35~450ĪŻ
1.5 ČŠąį─ŻöMĘĮĘ©
ČŠąį─ŻöM└¹ė├├└ć°Łh▒Ż╩ķ_░lĄ─ECOSAR│╠ą“Ż¼į┌▄ø╝■ųą▌ö╚ļ«a╬’Ą─ĮYśŗ╩ĮŻ¼▄ø╝■═©▀^ėŗ╦Ń╬’┘|Ą─č§╗»Ė▒«a╬’╝░╗»īWĮYśŗüĒėŗ╦ŃŲõ╔·æBČŠąįŻ¼┐╔ęįįu╣└ī”¶~ŅÉĪó╦«įķ║═ŠGįÕĄ─╝▒ąįĪó┬²ąįČŠąįĪŻ
1.6 ģf═¼ę“ūėėŗ╦ŃĘĮĘ©
ę²╚ļģf═¼ę“ūė(R)üĒČ©┴┐įu╣└UV/NaClO║═UV/SPC¾wŽĄ╚ź│²SAĄ─ģf═¼ą¦æ¬Ż¼ė╔╩Į(1)~╩Į(2)üĒ├Ķ╩÷ĪŻ═©▀^ėŗ╦ŃRUV/NaClO║═RUV/SPCįu╣└▓╗═¼ę“╦žī”ģf═¼ą¦æ¬Ą─ė░ĒæĪŻ

╩ĮųąŻ║RUV/NaClO║═RUV/SPCĘųäe×ķUV/NaClO║═UV/SPC¾wŽĄĄ─ģf═¼ę“ūėŻ╗kUV/NaClO×ķUV/NaClOĮĄĮŌSAĄ─öMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄŻ¼min−1Ż╗kUV/SPC×ķUV/SPCĮĄĮŌSAĄ─öMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄŻ¼min−1Ż╗kNaClO×ķNaClOĮĄĮŌSAĄ─öMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄŻ¼min−1Ż╗kSPC×ķSPCĮĄĮŌSAĄ─öMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄŻ¼min−1Ż╗kUV×ķUVĮĄĮŌSAĄ─öMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄŻ¼min−1ĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 UV/NaClO║═UV/SPC╣ż╦ćī”SAĄ─╚ź│²ī”▒╚
ī”▒╚┐╝▓ņ┴╦UVĪóNaClOĪóSPCĪóUV/NaClO║═UV/SPCī”SAĄ─╚ź│²Ż¼ĮY╣¹╚ńłD1╦∙╩ŠĪŻį┌Ę┤æ¬10minĢrŻ¼NaClO║═SPCī”SAĄ─╚ź│²┬╩āH×ķ4.5%║═2.5%Ż¼UVī”SAĄ─╚ź│²┬╩×ķ13%ĪŻUV/NaClO║═UV/SPCī”SAĄ─╚ź│²┬╩Ęųäe▀_ĄĮ82.2%║═92.3%Ż¼ŲõöMę╗╝ēĘ┤æ¬äė┴”īW│ŻöĄ(kobs)Ęųäe×ķ0.1732min−1║═0.2588min−1Ż¼×ķNaClO║═SPCĮĄĮŌSAĄ─37.6▒Č║═95.8▒ČĪŻ▀@šf├„UV┼cč§╗»ä®Ą─ģf═¼ū„ė├┤¾┤¾╠ßĖ▀┴╦SAĄ─╚ź│²┬╩ĪŻUV/NaClO║═UV/SPCĄ─RĘųäe▀_ĄĮ9.5║═15.9Ż¼įŁę“╩ŪUV/NaClO╣ż╦ćųą«a╔·┴╦ĪżOH║═RCS(╩Į(3)~╩Į(8))Ż¼UV/SPC╣ż╦ćųą«a╔·┴╦ĪżOHĪóO2Īż−║═CO3Īż-(╩Į(9)~╩Į(15))Ż¼ūįė╔╗∙Ą─«a╔·┐╔’@ų°╠ßĖ▀SAĄ─╚ź│²┬╩ĪŻ


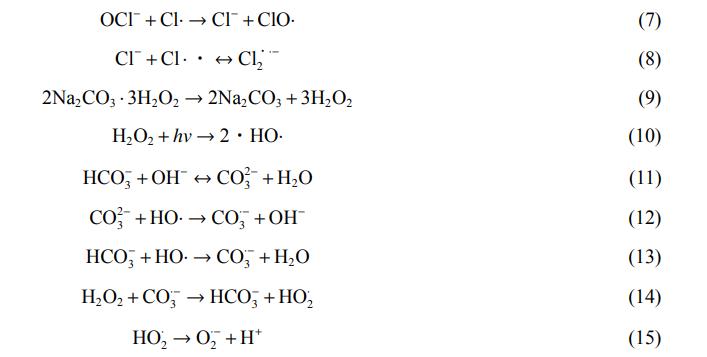
2.2 ▓╗═¼ė░Ēæę“ūėī”UV/NaClO║═UV/SPC╣ż╦ć╚ź│²SAĄ─ė░Ēæ
1)č§╗»ä®═Č╝ė┴┐ī”ĮĄĮŌSAĄ─ė░ĒæĪŻ╗∙ė┌UVĄ─AOPųąč§╗»ä®ØŌČ╚ī”ėąÖC╬█╚Š╬’ĮĄĮŌėąųžę¬ė░ĒæŻ¼┐╝▓ņ┴╦NaClO║═SPCØŌČ╚ī”SAĮĄĮŌĄ─ė░ĒæŻ¼kobs║═RļSNaClO║═SPCØŌČ╚Ą─ūā╗»╚ńłD2╦∙╩ŠĪŻė╔łD2┐╔ęŖŻ¼UV/NaClO╣ż╦ćųąNaClOĄ─═Č╝ė┴┐Å─1mg·L−1į÷╝ėų┴5mg·L−1Ż¼kobsÅ─0.0842min−1į÷╝ėų┴0.4378min−1Ż¼RUV/NaClOÅ─4.6į÷╝ėų┴24Ż╗UV/SPC╣ż╦ćųąSPCĄ─═Č╝ė┴┐Å─4mg·L−1į÷╝ėų┴20mg·L−1Ż¼kobsÅ─0.1239min−1į÷╝ėų┴0.3794min−1Ż¼RUV/SPCÅ─7.6į÷╝ėų┴23.2ĪŻ2ĘN╣ż╦ć╚ź│²SAĄ─kobs┼cRŠ∙ļSų°č§╗»ä®═Č╝ė┴┐Ą─į÷╝ėČ°į÷┤¾ĪŻ▀@╩Ūę“×ķč§╗»ä®Ą─į÷╝ė┐╔«a╔·Ė³ČÓūįė╔╗∙Ż¼▀MČ°╠ßĖ▀┴╦kobs┼cR ĪŻR║═kobsļSNaClO║═SPC═Č╝ė┴┐Ą─į÷╝ė│╩ŽÓ═¼Ą─ūā╗»┌ģä▌Ż¼ė╔ė┌NaClO║═SPCļyęį╚ź│²SAŻ¼▀@ę▓▒Ē├„┴╦SAĄ─╚ź│²ų„ę¬Üwę“ė┌ģf═¼ū„ė├ĪŻ
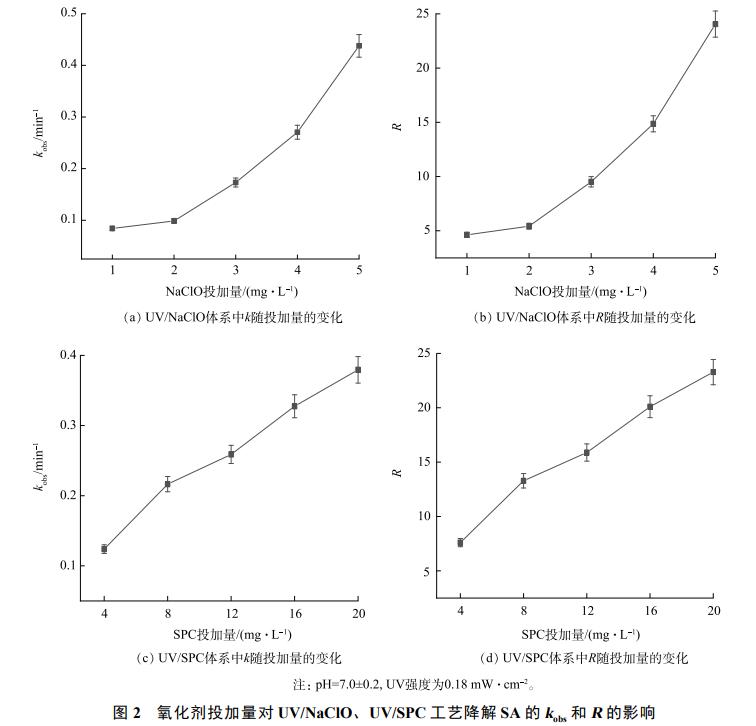
ųĄĄ├ūóęŌĄ─╩ŪŻ¼UV/SPC╣ż╦ćĄ─kobsį÷╦┘ļSSPC═Č╝ė┴┐Ą─į÷╝ėūāŠÅĪŻ▀Mę╗▓Įį÷┤¾SPCĄ─═Č╝ė┴┐(20~28mg·L−1)Ż¼SAĄ─╚ź│²┬╩ė╔97.8%╠ß╔²ų┴99.1%Ż¼«öSPCĄ─═Č╝ė┴┐┤¾ė┌28mg·L−1ĢrŻ¼SAĄ─╚ź│²┬╩ķ_╩╝Ž┬ĮĄŻ¼▓óūŅĮK▒Ż│ųį┌╝s95%(łD3)ĪŻ▀@╩Ūę“×ķ▀^┴┐Ą─SPC╔·│╔┴╦┤¾┴┐Ą─CO32-Ż¼Č°CO32-Ģ■Ž¹║─╚▄ę║ųąĄ─ĪżOHÅ─Č°ĮĄĄ═kobs(╩Į(9)~(13))ĪŻGUOĄ╚蹊┐O3╗Ņ╗»SPCĮĄĮŌ╦«ųą╗Ū░Ę╝ūÉ║▀“(SMX)Ģr═¼śė░l¼F▀^┴┐Ą─SPCĢ■ĮĄĄ═SMXĄ─╚ź│²┬╩ĪŻ
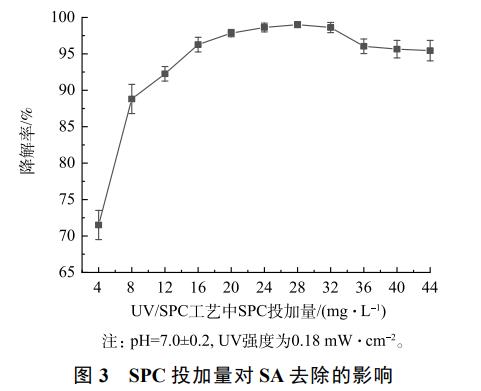
2)│§╩╝pHī”ĮĄĮŌSAĄ─ė░ĒæĪŻpH╩ŪAOPsųąųžę¬Ą─ė░Ēæę“╦žŻ¼×ķ┤╦Ż¼╠ĮŠ┐┴╦▓╗═¼pHŽ┬UV/NaClO║═UV/SPC╣ż╦ćī”SAĄ─╚ź│²(łD4)ĪŻ╚ńłD4Ż¼│§╩╝pHī”SA╚ź│²ėą’@ų°Ą─ė░ĒæĪŻļSų°pHÅ─11Ž┬ĮĄų┴3Ż¼UV/NaClO╣ż╦ćųąkobsÅ─0.1017min−1ų▓Į╔²ų┴0.2876min−1Ż¼RUV/NaClOÅ─5.6į÷ų┴15.8ĪŻČ°UV/SPC╣ż╦ćųąkobs║═RUV/SPCį┌pH×ķ7ĢrūŅ┤¾Ż¼▀_ĄĮ0.2889min−1║═17.5Ż¼kobs┼cRUV/SPCätļSų°pHĄ─į÷┤¾╗“£pąĪČ°£pąĪĪŻ«öpH×ķ11ĢrŻ¼kobs║═RUV/SPCĘųäeĮĄĄ═×ķ0.1502min−1║═9.4Ż╗«öpH×ķ3ĢrŻ¼kobs┼cRUV/SPCĘųäeĮĄų┴0.0834min−1║═5.2Ż╗
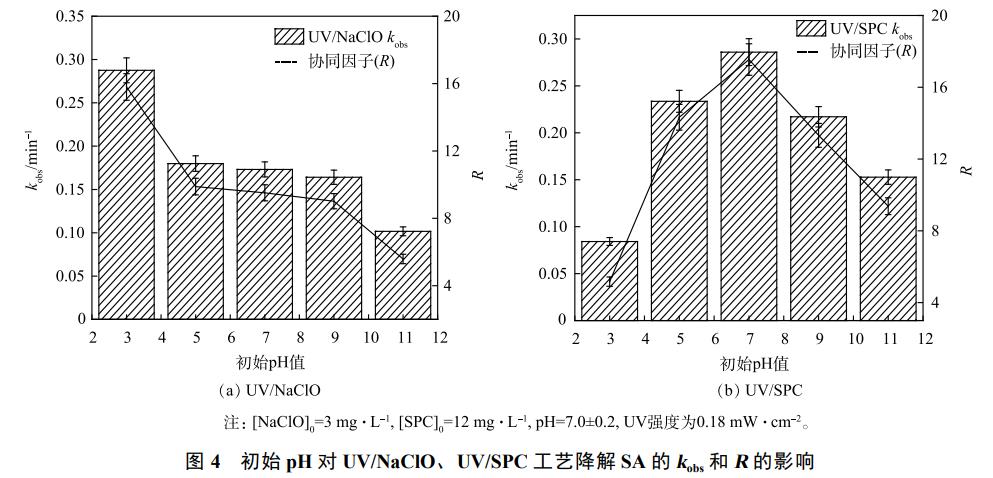
pH┐╔═©▀^ė░ĒæNaClO╚▄ė┌╦«║¾HOCl║═ClO−Ą─┤µį┌ą╬╩Į▀MČ°ė░ĒæUV/NaClO╣ż╦ćī”Ą─SAĄ─╚ź│²Ż¼HOCl║═ClO−į┌254nm╠ÄĄ──”Ā¢╬³╣ŌŽĄöĄŽÓ═¼Ż¼pHąĪė┌7.5ĢrŻ¼╚▄ę║ųąų„ę¬ęįHOClĄ─ą╬╩Į┤µį┌Ż¼Č°pH┤¾ė┌7.5ĢrŻ¼ų„ę¬ęįClO−Ą─ą╬╩Į┤µį┌ĪŻSA╩Ūę╗ĘN╚§╦߯¼╚▄ė┌╦«ųąĢr┐╔ęįļŖļx│÷H+Ż¼═¼ĢrSAūā×ķSA−ĪŻę“┤╦╚▄ę║pHįĮ┤¾ClO−┼cSA−║¼┴┐Š∙Ģ■į÷╝ėŻ¼ā╔š▀ļŖ║╔ŽÓ═¼«a╔·┼┼│Ōī¦ų┬kobsŽ┬ĮĄĪŻCAOĄ╚蹊┐UV/NaClO╣ż╦ćĮĄĮŌī”ęꧯ░▒╗∙Ęė(AAP)Ģr═¼śėĄ├│÷┴╦╚▄ę║pHį÷┤¾ĢrAAP−┼cClO−Ą─┼┼│Ōī¦ų┬AAPĄ─ĮĄĮŌ╦┘┬╩Ž┬ĮĄĄ─ĮYšōĪŻ
ļSų°pHĄ─į÷╝ėŻ¼ĪżOHč§╗»ļŖ╬╗Å─2.62VŽ┬ĮĄų┴2.15VŻ¼═¼ĢrĪżOH┼c╚▄ę║ųą┤µį┌Ą─OH−Ę┤æ¬╔·│╔č§╗»ļŖ╬╗×ķ1.78VĄ─OĪż−ĪŻ«öpHąĪė┌7ĢrŻ¼kobs┼cRUV/SPCļSų°pHĄ─£pąĪČ°ĮĄĄ═Ż¼įŁę“╩Ū╦ßąį¾wŽĄųąSAų„ę¬ęįĘųūėĄ─ą╬╩Į┤µį┌Ż¼Š▀ėąę╗Č©Ą─╩Ķ╦«ąįŻ¼╣╩kobsļSų°pHĄ─ĮĄĄ═Č°ĮĄĄ═Ż¼PANDAĄ╚蹊┐┬Ģ╣Ō┤▀╗»SPCĮĄĮŌč§Ę·╔│ąŪ(OFX)Ģr░l¼F▓╗═¼pHŽ┬╬█╚Š╬’Ą─╚ź│²┬╩ĪóĮĄĮŌ╦┘┬╩┼c╬█╚Š╬’Ą─ėH╦«Īó╩Ķ╦«ąįėąĻPĪŻ┤╦═ŌŻ¼HPESHIĄ╚ęįSPCū„×ķč§╗»ä®ĮĄĮŌOFXę▓═¼śėĄ├│÷┴╦į┌pH×ķųąąįĢrĘ┤æ¬╦┘┬╩┼c╚ź│²┬╩ūŅ╝čĄ─ĮYšōĪŻ
3)NO3−ī”ĮĄĮŌSAĄ─ė░ĒæĪŻ╠ņ╚╗╦«ŁhŠ│ųąŲš▒ķ║¼ėąNO3©CŻ¼Ųõ┘|┴┐ØŌČ╚×ķ0.3mg·L−1ĪŻ×ķ╠ĮŠ┐Ųõė░ĒæŻ¼īŹ“×ųą┐╝▓ņ┴╦╚▄ę║│§╩╝NO3−ØŌČ╚ī”SA╚ź│²Ą─ė░Ēæ(łD5)ĪŻ
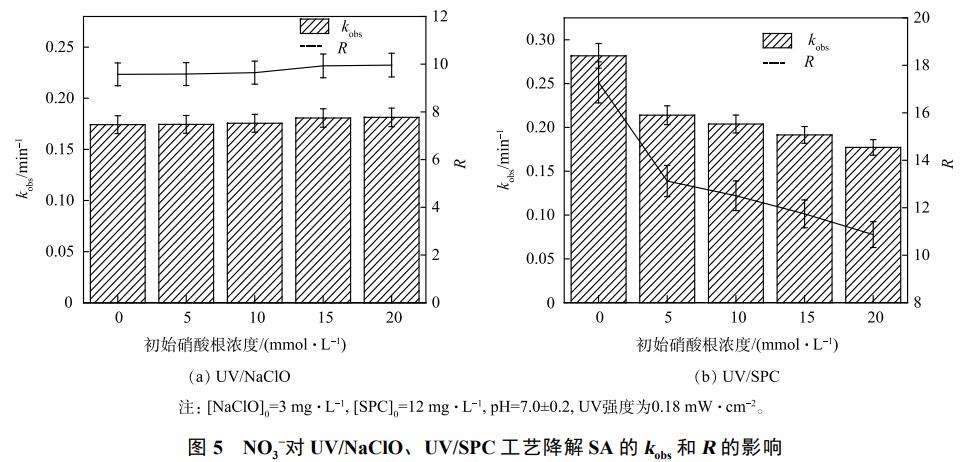
╚ńłD5╦∙╩ŠŻ¼NO3−ī”UV/NaClO╣ż╦ć╚ź│²SAėą▌p╬ó┤┘▀Mū„ė├Ż¼NO3−ØŌČ╚Å─0į÷╝ėų┴20mmol·L−1Ż¼kobsÅ─ė╔0.1742min−1į÷┤¾ų┴0.1813min−1Ż¼Rė╔9.5į÷ų┴9.9Ż¼kobs┼cRUV/NaClOį÷ķL▓╗’@ų°ĪŻUV▌ŚššNO3−┐╔╔·│╔Ž§╦ßĖ∙ūįė╔╗∙(NO3Īż-)║═ü厧╦ßĖ∙ūįė╔╗∙(NO2Īż-)Ż¼╚ń╩Į(16~17)╦∙╩ŠĪŻŲõųąNO3Īż-Ą─č§╗»ļŖ╬╗2.3~2.5VĄ═ė┌ĪżOHŻ¼NO2Īż-┐╔┼cĪżOH┐╔ęį▀Mę╗▓ĮĘ┤欎¹║─ĪżOH(╩Į(18))Ż¼ę“┤╦Ż¼UV/NaClO¾wŽĄųą╔┘┴┐┤µį┌Ą─ĪżOH┼c╚▄ę║ųąĄ─NO2Īż-Ę┤æ¬ĮĄĄ═ĪżOHĄ─ØŌČ╚Ż¼Ą½╩Ū╣ŌĮŌ╔·│╔Ą─NO3Īż-║═NO2Īż-╚įī”╚ź│²SAėą╦∙žĢ½IŻ¼╣╩kobs│╩¼F┬į╬óĄ─į÷┤¾ĪŻļSų°NO3−ØŌČ╚ė╔0į÷╝ėų┴20mmol·L−1Ż¼UV/SPC╣ż╦ćųąkobsė╔0.2817min−1ĮĄų┴0.1772min−1Ż¼RUV/SPCė╔17.3ĮĄĄ═ų┴10.8Ż¼NO3−ī”SAĄ─╚ź│²ėąęųųŲū„ė├Ż¼┐╔─▄Ą─įŁę“╩ŪUV/SPC╣ż╦ć¾wŽĄųąĪżOHī”ĮĄĮŌŲų°ų„꬞Ģ½IŻ¼Č°NO3−Ą─╝ė╚ļīó┤¾┴┐╔·│╔Ą─ĪżOH▐D╗»×ķč§╗»ąį▌^╚§Ą─NO3Īż-╝░Ųõ╦¹«a╬’(╩Į(16)~╩Į(18))Ż¼ę“┤╦UV/SPC╣ż╦ćĄ─╚ź│²┬╩┼cĘ┤æ¬╦┘┬╩Š∙╩▄ĄĮ┴╦ĮĄĄ═║═ęųųŲĪŻ

4)HCO3−ī”ĮĄĮŌSAĄ─ė░ĒæĪŻHCO3− ÅVĘ║┤µį┌ė┌Ąž▒Ē╦«ųąŻ¼┐╔─▄Ģ■ė░ĒæĖ▀╝ēč§╗»╣ż╦ćųą╬█╚Š╬’Ą─ĮĄĮŌĪŻę“┤╦Ż¼┐╝▓ņ┴╦╚▄ę║│§╩╝HCO3−ØŌČ╚ī”SA╚ź│²Ą─ė░Ēæ(łD6)ĪŻ
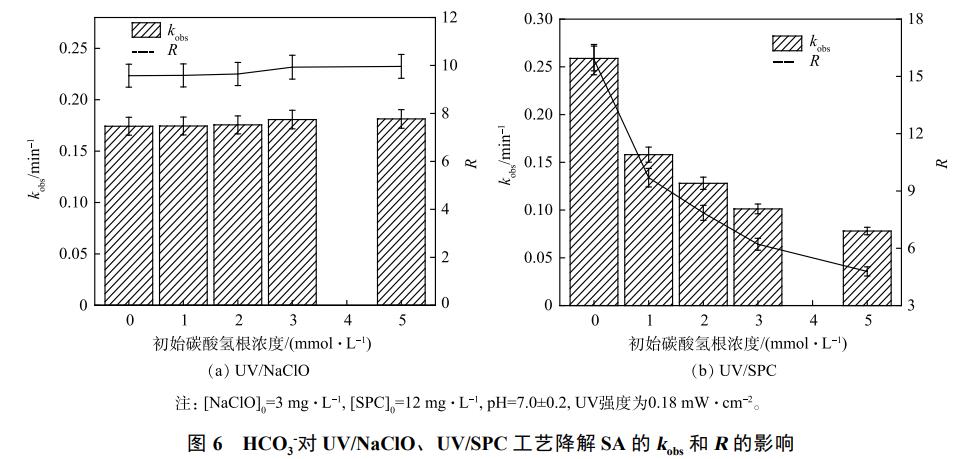
╚ńłD6╦∙╩ŠŻ¼UV/NaClO╣ż╦ćĄ─kobs║═RUV/NaClOļSHCO3−ØŌČ╚Ą─į÷╝ėČ°į÷┤¾Ż¼HCO3−Ą─ØŌČ╚ė╔0į÷╝ėų┴5mmol·L−1ĢrŻ¼kobsė╔0.1732min−1į÷╝ėų┴0.1813min−1Ż¼RUV/NaClOė╔9.5į÷╝ėų┴9.9Ż¼Ą½ā╔š▀į÷╝ėĘ∙Č╚▓╗├„’@ĪŻHCO3−║═CO32-Š∙─▄┼cĪżOHĘ┤æ¬╔·│╔CO3Īż-(╩Į(11)~╩Į(13))Ż¼UV/NaClO╣ż╦ć¾wŽĄųąHCO3−Ž¹║─┴╦«a╔·Ą─ĪżOHŻ¼Ą½UV/NaClO╣ż╦ćųąŲų„꬞Ģ½IĄ─×ķRCSŻ¼╣╩HCO3−ī”ĪżOHĄ─Ž¹║─▓óø]ėąĮĄĄ═kobsĪŻ┤╦═ŌŻ¼▐D╗»╔·│╔Ą─CO3Īż-ī”║¼ėą▒Į░ĘĄ╚Ė╗ļŖūėĄ─╬█╚Š╬’Š▀ėą▀xō±ąįŻ¼▀@┐╔─▄┤┘▀M┴╦SAĄ─ĮĄĮŌĪŻŠC║ŽĪżOHĄ─Ž¹║─┼cCO3Īż-Ą─╔·│╔Ż¼īŹ“×ųąSA╚ź│²┬╩▓╗ūāŻ¼kobs║═RUV/NaClOį÷╝ė▓╗├„’@Ą─¼FŽ¾ĪŻZHUĄ╚蹊┐UV/NaClO╣ż╦ćĮĄĮŌ┐©±R╬„ŲĮ(CBZ)═¼śėĄ├│÷┴╦HCO3−ī”CBZ╚ź│²ė░Ēæ▌^ąĪĄ─ĮYšōĪŻ
HCO3−ī”UV/SPC╣ż╦ćSAĄ─╚ź│²ŲęųųŲū„ė├ĪŻ«öHCO3−Ą─ØŌČ╚Å─0į÷╝ėų┴5mmol·L−1Ż¼kobsė╔0.2588min−1ĮĄų┴0.0780min−1Ż¼ŽÓæ¬Ą─RUV/SPCė╔15.8ĮĄų┴4.7Ż¼ā╔š▀Ž┬ĮĄĘ∙Č╚├„’@ĪŻ▓╗═¼ė┌UV/NaClO╣ż╦ćŻ¼UV/SPC╣ż╦ć╚▄ę║ųą▒Š╔Ē┤µį┌HCO3−┼cCO32-Ż¼╣╩¾wŽĄųąĢ■«a╔·CO3Īż-Ż¼╚╗Č°UV/SPC╣ż╦ćųąĄ─ėąą¦č§╗»ä®×ķH2O2Ż¼CO3Īż-┐╔ęį┼cH2O2Ę┤æ¬▓óŽ¹║─H2O2(╩Į(19))ĪŻ┤╦═ŌŻ¼╚▄ę║ųąHCO3−┼cCO32-┼cĘ┤æ¬╔·│╔Ą─ĪżOH(╩Į(11)~╩Į(13))Ę┤æ¬Ż¼╔·│╔Ą─CO3Īż-▀Mę╗▓ĮŽ¹║─H2O2Ż¼╣╩ļSų°HCO3−ØŌČ╚Ą─į÷╝ėŻ¼kobs║═RUV/SPCŠ∙├„’@Ž┬ĮĄĪŻ
H2O2+CO3⋅−Ī·HCO3−+HO2⋅ (19)
5)Ė»ų│╦ßī”ĮĄĮŌSAĄ─ė░ĒæĪŻNOM╩Ū╠ņ╚╗╦«ŁhŠ│ųąŲš▒ķ┤µį┌Ą─ę╗ĘNėąÖCĮMĘųŻ¼īŹ“×ųą▓╔ė├Ė»ų│╦ß(HA)─ŻöMėąÖC╬’Ż¼┐╝▓ņ┴╦HAī”SA╚ź│²Ą─ė░Ēæ(łD7)ĪŻ
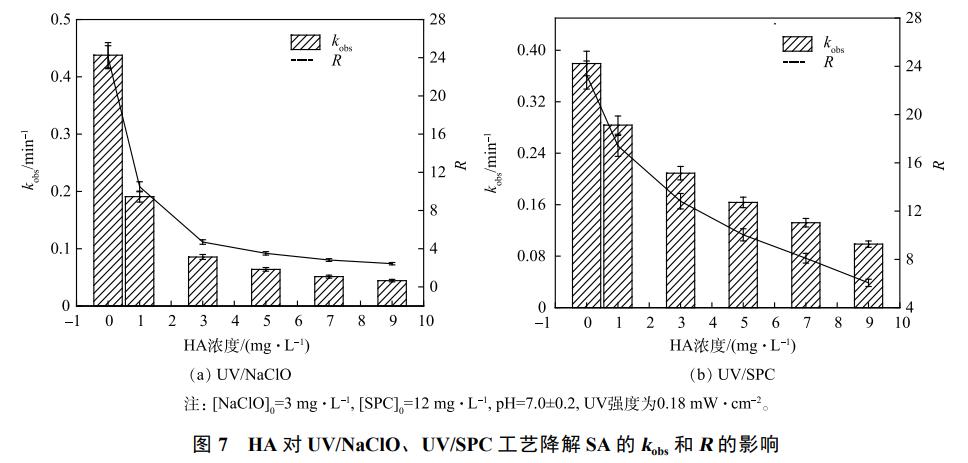
╚ńłD7╦∙╩ŠŻ¼HAī”2ĘN╣ż╦ć╚ź│²SAŠ∙ėą├„’@Ą─ęųųŲū„ė├ĪŻ«öHAĄ─┘|┴┐ØŌČ╚ė╔0į÷╝ėų┴9mg·L−1Ż¼UV/NaClO╣ż╦ćĄ─kobsÅ─0.4378min−1Ž┬ĮĄų┴0.0443min−1Ż¼RUV/NaClOätÅ─24ĮĄų┴2.4Ż╗UV/SPC╣ż╦ćĄ─kobsÅ─0.3794min−1Ž┬ĮĄų┴0.0987min−1Ż¼RUV/SPCÅ─23.2ĮĄų┴6ĪŻHA╩Ū╠ņ╚╗ėąÖC╬’(NOM)Ą─Ąõą═┤·▒ĒŻ¼Ųõī”2ĘN╣ż╦ćkobsĄ─ęųųŲėąŽÓ═¼Ą─įŁę“Ż║(1)UV«a╔·Ą─╣Ōūėį┌╚ļ╔õĢr▒╗HA╬³╩š┴╦Ż¼ī¦ų┬SAĄ─╣ŌĮĄĮŌą¦┬╩ĮĄĄ═Īóč§╗»ä®Ą─╝ż╗Ņ╣ŌūėöĄ┴┐£p╔┘Ż╗(2)HAŠ▀ėąŪÕ│²ū„ė├Ż¼Ž¹║─╚▄ę║ųą╝ż░l«a╔·Ą─ūįė╔╗∙Ż¼ĮĄĄ═ūįė╔╗∙Ą─ØŌČ╚ĪŻLIĄ╚╚╦蹊┐UV/NaClOĮĄĮŌ╦«ųąļp┬╚Ęę╦ßŌc(DS)Ģr╠ĮŠ┐NOMī”DSĮĄĮŌĄ─ė░ĒæŻ¼═¼śėĄ├│÷┴╦NOMĢ■ęųųŲDSĮĄĮŌĄ─ĮYšōĪŻ
2.3 UV/NaClO║═UV/SPC╣ż╦ć╚ź│²SAĄ─ÖCųŲ┼cĮĄĮŌ┬ĘÅĮ
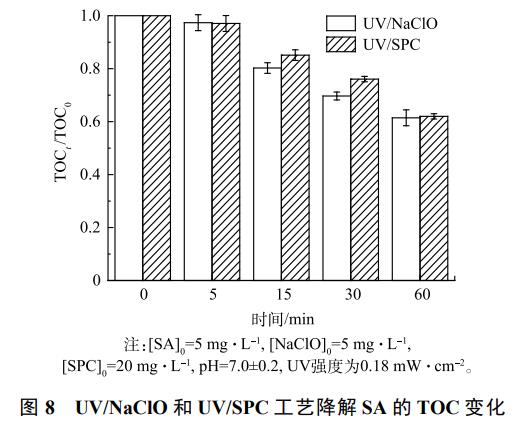
1)TOCĘų╬÷ĪŻUV/NaClO║═UV/SPC╣ż╦ćĮĄĮŌSAĄ─▀^│╠ųą╚▄ę║TOCĄ─ūā╗»Ūķør╚ńłD8╦∙╩ŠĪŻė╔łD8┐╔ų¬Ż¼15min║═30minĢrŻ¼UV/NaClO╣ż╦ćųąTOC╚ź│²┬╩Ęųäe×ķ20%║═31%Ż¼Č°UV/SPC╣ż╦ćųąTOC╚ź│²┬╩ätĘųäe×ķ15%║═24%Ż¼60min║¾2ĘN╣ż╦ćTOCĄ─╚ź│²(ĄV╗»Č╚)Š∙į┌40%ū¾ėęĪŻUV/NaClO╣ż╦ćī”TOCĄ─╚ź│²┬įā×ė┌UV/SPC╣ż╦ćĪŻ╚▄ę║TOCĄ─╚ź│²╩Ūę“×ķUV/NaClO║═UV/SPC╣ż╦ć«a╔·Ą─ūįė╔╗∙īóSAč§╗»×ķCO2║═H2OŻ¼╚╗Č°īŹ“×ĮY╣¹▒Ē├„SA╚ź│²║¾▓óø]ėą═Ļ╚½▐D╗»×ķCO2║═H2OŻ¼Č°╩Ū╔·│╔┴╦Ųõ╦¹ėąÖCĖ▒«a╬’ĪŻPATILĄ╚ī”▒╚蹊┐┴╦│¼┬Ģ/H2O2Īó╣ŌĘęŅDĪó│¼┬Ģ/╣ŌĘęŅDĄ╚╣ż╦ćī”ÓżŽxļ▀(ACP)Ą─╚ź│²▒Ē├„┤╦ŅÉAOPsļyęįīó╬█╚Š╬’═Ļ╚½ĄV╗»ĪŻėąčąŠ┐▒Ē├„Ż¼╝ė┤¾č§╗»ä®Ą─ØŌČ╚╗“š▀╠ßĖ▀UVĄ─╣”┬╩┐╔ęį╠ßĖ▀ĄV╗»Č╚Ż¼įōĘĮĘ©┐╔×ķ║¾└mį┌īŹļH╠Ä└Ē╦«ųą═Ļ╚½ĄV╗»PPCPs╠ß╣®ģó┐╝ĪŻ
2)DFTėŗ╦ŃĪŻīóSAĮYśŗā×╗»▓óŠÄ╠¢╚ńłD9Ż¼▓ó▀MąąDFTėŗ╦ŃŻ¼ĮY╣¹ęŖ▒Ē1ĪŻĘųūėų«ķgĄ─Ę┤æ¬ÖC└Ēų„ę¬░³└©ėH║╦Ę┤æ¬ĪóėHļŖĘ┤æ¬║═ūįė╔╗∙╣źō¶Ę┤æ¬Ż¼į┌AOPsųąų„ę¬╩Ūūįė╔╗∙┼cPPCPsų«ķgĄ─ėHļŖĘ┤æ¬ĪŻŲõųąĖŻŠ«ųĖöĄ┐╔ęįĘ┤æ¬Ė„éĆįŁūė╬╗³cęū╩▄╣źō¶Ą─ĘNŅÉŻ¼ų„ę¬░³└©Ż║ėH║╦╣źō¶(f+)ĪóėHļŖ╣źō¶(f-)║═ūįė╔╗∙╣źō¶(f0)Ż¼ŪęĖŻŠ«ųĖöĄįĮ┤¾Ż¼▒Ē├„įōįŁūė╬╗³c╩Ūų„ꬥ─▀M╣źļŖ╬╗ĪŻĖ∙ō■DFTėŗ╦ŃĮY╣¹Ż¼ęū╩▄╣źō¶Ą─ļŖ╬╗ų„ę¬╩ŪC║═OĪŻŲõųąO4ĪóC7ęū╩▄ėHļŖ╣źō¶Ż¼C1ĪóC6║═C7ęū╩▄ėH║╦╣źō¶Ż¼O4ĪóC6║═O9ęū╩▄ūįė╔╗∙╣źō¶ĪŻ┐╔ęį┐┤│÷ęū╩▄╣źō¶Ą─ļŖ╬╗ų„ę¬╝»ųąį┌SAĘė┴u╗∙Īó¶╚╗∙Ą─Ą─ī”╬╗║═ķg╬╗Ż¼DFTĄ─ĮY╣¹×ķĘų╬÷SAĮĄĮŌ«a╬’┼c┬ĘÅĮ╠ß╣®└Ēšōę└ō■ĪŻ
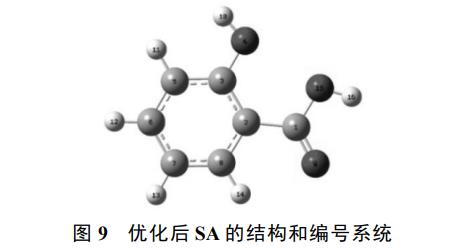
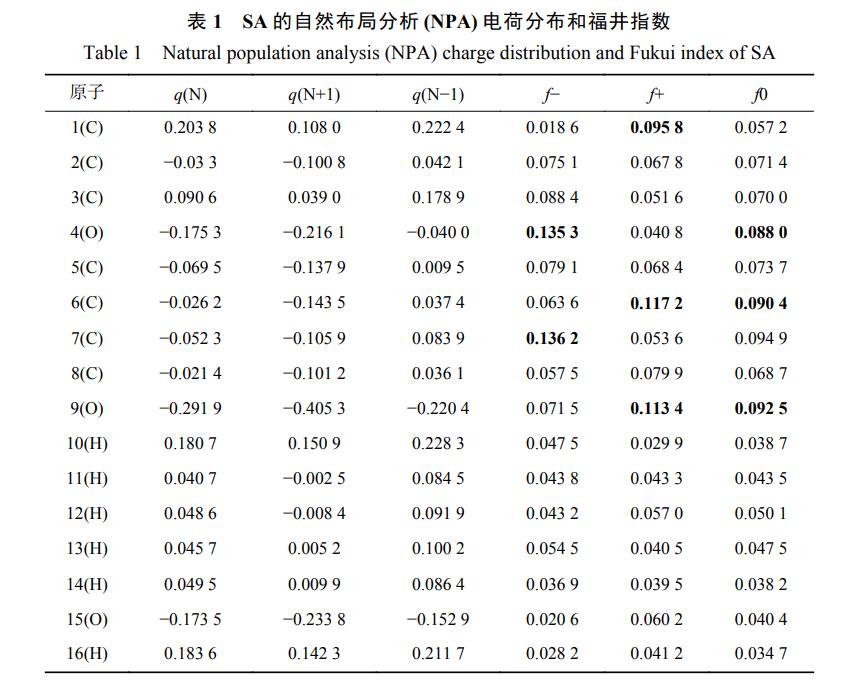
3)ĮĄĮŌ┬ĘÅĮĘų╬÷ĪŻŠC║ŽGC-MS║═LC-MSĮY╣¹▓óĮY║Ž┤╦Ū░DFTĄ─Ęų╬÷ĮY╣¹Ż¼═Ų£ySAį┌2ĘN╣ż╦ćū„ė├Ž┬┐╔─▄Ą─ĮĄĮŌ┬ĘÅĮ╚ńłD10╦∙╩ŠĪŻUV/NaClO╣ż╦ćųąSAų„ꬫa╬’ėą┬╚┤·«a╬’(m/z 172.90Īó178.98Īó197.94)Ż¼Ųõ×ķRCS║═NaClOĄ─č§╗»ĮY╣¹ĪŻį┌2éĆ╣ż╦ćųąŠ∙│÷¼FĘė┴u╗∙(-OH)Ą─╚Ī┤·║═č§╗»Ż¼ų„ꬫa╬’ėą2,3-Č■┴u╝ū╗∙▒Į╝ū╦ß(2,3-DHBAŻ¼m/z 153.89)Īó2,4-Č■┴u╝ū╗∙▒Į╝ū╦ß(2,4-DHBA)Īó2,5-Č■┴u╝ū╗∙▒Į╝ū╦ß(2,5-DHBA)Īó2,6-Č■┴u╝ū╗∙▒Į╝ū╦ß(2,6-DHBA)Īó▒ĮĘė(m/z 93.9)ĪóÓÅ▒ĮČ■Ęė(m/z 110)Īó▀B▒Į╚²Ęė(m/z 126)Ą╚Ż¼┤╦ŅÉ«a╬’╩Ūė╔ė┌ĪżOHĄ╚ūįė╔╗∙Ą─č§╗»«a╔·Ą─ĪŻįōĮY╣¹┼c┤╦Ū░ł¾Ą└Ą─SA┼cĪżOHĄ─Ę┤欫a╬’ŽÓę╗ų┬ĪŻ▀@ŅÉ«a╬’į┌ūįė╔╗∙Ą─č§╗»ū„ė├Ž┬▀Mę╗▓Į┐╔ęįĘųĮŌ×ķ╝ū╚®Īóęę╚®Īóęę╦ßĪó▓▌╦ߥ╚ėąÖCąĪĘųūėĪŻ┤╦═ŌŻ¼ųĄĄ├ūóęŌĄ─╩ŪŻ¼į┌UV/NaClO╣ż╦ćĄ─ĮĄĮŌSAĄ─«a╬’ųąÖz£y│÷┴╦╚²┬╚╝ū═ķ(TCM)Ż¼Ųõ×ķĄõą═Ą─DBPsŻ¼Š▀ėą╚²ų┬ū„ė├Ż¼ę“┤╦Ż¼ąĶę²ŲųžęĢĪŻ
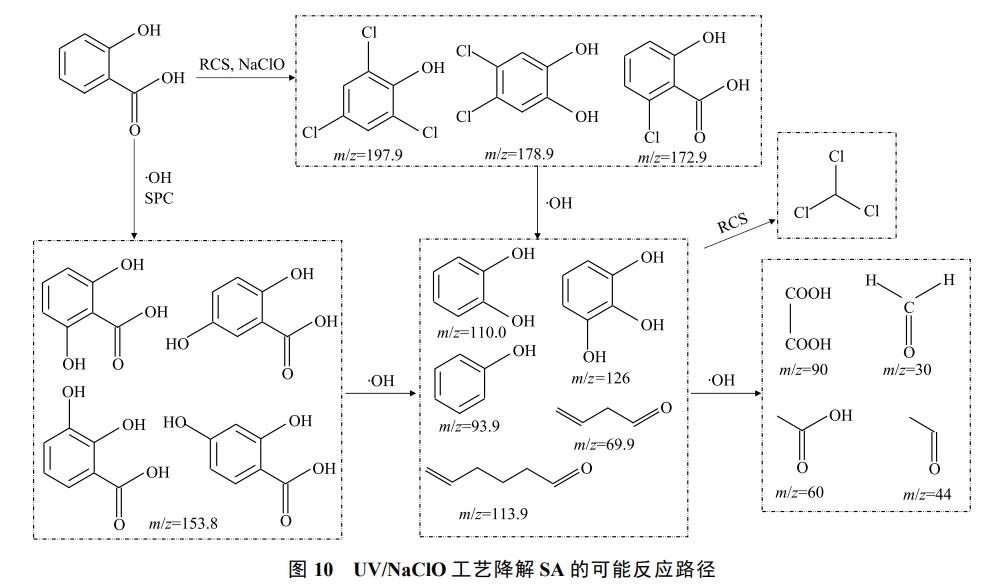
4)«a╬’ČŠąįĘų╬÷ĪŻ═©▀^ECOSAR▄ø╝■ī”ęčĶbČ©«a╬’▀Mąą┴╦ČŠąį─ŻöMŻ¼ČŠąįĄ─įu╣└Ą╚╝ēĘų4ŅÉŻ║LC50ĪóEC50╗“ChV>100mg·L−1Ģr×ķ¤oČŠŻ╗100mg·L−1Ī▌LC50ĪóEC50╗“ChV>10mg·L−1Ģr×ķėą║”Ż╗10mg·L−1 Ī▌LC50ĪóEC50╗“ChV>1mg·L−1Ģr×ķėąČŠŻ╗LC50ĪóEC50╗“ChVĪ▄1mg·L−1Ģr×ķäĪČŠĪŻŲõųąChV┤·▒Ē┬²ąįČŠąįŻ╗LC50┤·▒Ē░ļöĄų┬╦└ØŌČ╚Ż¼╝┤į┌äė╬’╝▒ąįČŠąįīŹ“×ųąŻ¼╩╣╩▄įćäė╬’░ļöĄ╦└═÷Ą─ČŠ╬’ØŌČ╚Ż╗EC50ųĖ░ļöĄą¦æ¬ØŌČ╚Ż¼═©▀^£yČ©╣żśIÅU╦«║═Ųõ╦¹╗»īW╬’┘|ī”¶~ŅÉĄ╚╦«╔·╔·╬’Ą─╝▒ąįČŠąįīŹ“×ĘĮĘ©Ż¼ęįį┌ę╗Č©▒®┬ČĢrķgā╚Ą─ŲĮŠ∙─═╩▄Ž▐(TLm)▒Ē╩ŠŻ╗TLm┤·▒Ēį┌╝▒ąįČŠąįīŹ“×ųą╩╣╩▄įć╦«╔·äė╬’░ļöĄ┤µ╗Ņ╗“░ļöĄ╦└═÷Ą─ČŠ╬’ØŌČ╚Ż¼╝┤TLm═¼EC50ĪŻ
SAĄ─¶~Īó╦«įķ║═ŠGįÕĄ─ChVųĄĘųäe×ķ12.98Īó7.06║═25.55mg·L−1Ż¼Ė∙ō■įu╣└Ą╚╝ēĘųäe┼ąČ©×ķėą║”ĪóėąČŠ║═ėą║”ĪŻė╔łD11┐╔ęŖŻ¼SAĄ─ĮĄĮŌ«a╬’│÷¼F┴╦įu╣└Ą╚╝ē×ķäĪČŠĄ─╬’┘|Ż¼Ųõųą2,5-DHBA╩ŪŲõ═¼Ęų«Éśŗ«a╬’ųąČŠąįūŅÅŖĄ─Ż¼Ųõ¶~ŅÉĄ─ChVųĄ×ķ0.10mg·L−1Ż¼×ķäĪČŠĄ╚╝ēĪŻm/z 69.9ī”¶~ŅÉĄ─LC50,96h║═ChVųĄę▓▀_ĄĮ┴╦äĪČŠĄ╚╝ēĪŻ▒ĮĘėĪóm/z 113.9Īó╝ū╚®║═ęę╚®į┌╦«įķĄ─ChVįu╣└═¼śė×ķäĪČŠĄ╚╝ēŻ¼ÓÅ▒ĮČ■ĘėĪó▀B▒Į╚²Ęė║═m/z 197.9ī”ŠGįÕĄ─ChVįu╣└ę▓▀_ĄĮ┴╦äĪČŠĄ╚╝ēĪŻųĄĄ├ūóęŌĄ─╩ŪŻ¼m/z 197.9į┌¶~Īó╦«įķ║═ŠGįÕ3éĆ╔·╬’ČŠąįįu╣└ųąŠ∙▀_ĄĮ┴╦äĪČŠĄ╚╝ēĪŻ▒╗šJ×ķŠ▀ėą╚²ų┬ū„ė├Ą─TCMį┌╝▒ąįČŠąįįu╣└ųąČŠąįąĪė┌SAŻ¼┐╔─▄Ą─įŁę“╩ŪTCMĄ─ČŠąį▒Ē¼F×ķ▀zé„╗“╗∙ę“ČŠąįŻ¼╣╩▓ó╬┤į┌╝▒ąįČŠąįųą▒Ē¼F│÷ČŠąįĪŻį┌░l╣Ō╝ÜŠ·╝▒ąįČŠąįųąŻ¼SA│§╩╝╚▄ę║ī”░l╣Ō╝ÜŠ·ø]ėąęųųŲŻ¼UV/NaClO╣ż╦ćųąĘ┤æ¬╚▄ę║Ą─ŽÓī”ęųųŲ┬╩Ž╚į÷╝ėĄĮ100%į┘ĮĄų┴63%Ż¼UV/SPC╣ż╦ćųąĘ┤æ¬╚▄ę║ŽÓī”ęųųŲ┬╩į┌Ę┤æ¬ķ_╩╝═¼śėŽ╚į÷╝ėĄĮ50%▓óų▓Įķ_╩╝Ž┬ĮĄ(Ę┤æ¬20minĢrĮĄų┴35%)ĪŻČŠąį─ŻöMįu╣└×ķ░l╣Ō╝ÜŠ·╝▒ąįČŠąįīŹ“×ųąSAĮĄĮŌ║¾╝▒ąįČŠąį┤¾ė┌SA╚▄ę║│§╩╝ČŠąį╠ß╣®┴╦ū¶ūCĪŻ«a╬’m/z 172.9║═╝ū╦ßįu╣└ĮY╣¹Š∙×ķ¤oČŠŻ¼įōĮY╣¹═¼śė“×ūC┴╦ļSų°ĮĄĮŌĄ─▀MąąŻ¼«a╬’│§▓ĮĮĄĮŌ×ķąĪĘųūė╬’┘|Ż¼╚▄ę║Ą─╝▒ąįČŠąįķ_╩╝ų▓ĮŽ┬ĮĄĪŻį┌║¾└mĄ─蹊┐┼cæ¬ė├ųąŻ¼┐╔ęį▀Mę╗▓Į╝ė┤¾ī”«a╬’Ą─Öz£y┼cČŠąįįu╣└Ż¼▓ó▀m«öčėķLĮĄĮŌĄ─ĢrķgŻ¼┐╔ęįėąą¦ĮĄĄ═╚▄ę║Ą─╝▒ąįČŠąįĪŻ
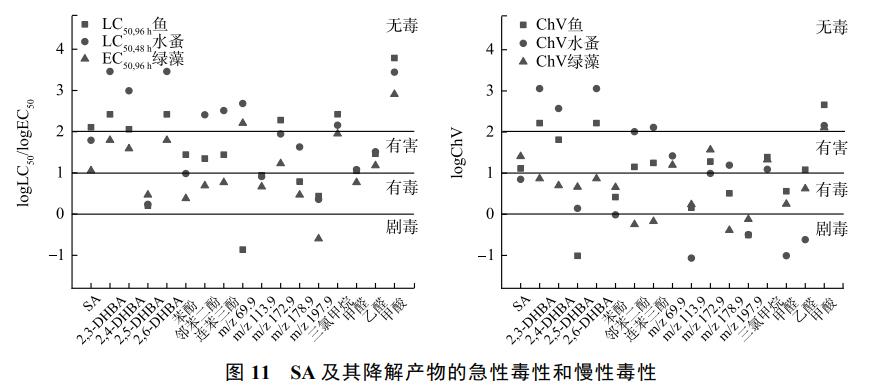
3ĪóĮYšō
1)UV/NaClO║═UV/SPC╣ż╦ćėąą¦╠ßĖ▀┴╦SAĄ─╚ź│²ą¦┬╩Ż¼2ĘN╣ż╦ćĄ─RĘųäe▀_ĄĮ9.5║═15.9ĪŻUV/SPC╣ż╦ćį┌TOC╚ź│²║═¤╔╣ŌÅŖČ╚ĮĄĄ═ĘĮ├µ│╩¼Fę╗Č©Ą─ā×ä▌ĪŻļSų°č§╗»ä®═Č╝ė┴┐Ą─į÷╝ė2ĘN╣ż╦ćĄ─ĮĄĮŌą¦┬╩║═RŠ∙ų▓Į╠ßĖ▀Ż¼Ą½▀^┴┐Ą─SPCĢ■ęųųŲSAĄ─╚ź│²ĪŻ
2)│§╩╝pHī”2ĘN╣ż╦ćĄ─kobs║═RŠ∙ėą▌^┤¾Ą─ė░ĒæŻ¼ļSų°pHė╔11Ž┬ĮĄų┴3Ż¼UV/NaClO╣ż╦ćųąkobsė╔0.1017min−1ų▓Į╔²ų┴0.2876min−1Ż¼UV/SPC╣ż╦ćųąkobs║═RŠ∙į┌pH×ķ7Ģr×ķūŅ┤¾Ż¼Č°kobs┼cRŠ∙ļSų°pHĄ─į÷┤¾╗“£pąĪČ°£pąĪŻ╗NO3−┼cHCO3−ī”UV/NaClO╣ż╦ć╚ź│²SAėą┤┘▀Mū„ė├Ż¼Č°ī”UV/SPC╣ż╦ć╚ź│²SAėą├„’@Ą─ęųųŲū„ė├Ż╗HAī”2ĘN╣ż╦ć╚ź│²SAŠ∙ėąęųųŲĪŻ
3)SAį┌2ĘN╣ż╦ćųąĄ─ĮĄĮŌÖC└Ēų„ę¬×ķūįė╔╗∙Ą─╚Ī┤·║═č§╗»Ż¼ųĄĄ├ūóęŌĄ─╩ŪUV/NaClO╣ż╦ćĄ─ĮĄĮŌ«a╬’ųąÖz£y│÷┴╦Ąõą═Ą─DBPs╚²┬╚╝ū═ķĪŻ
4)▄ø╝■ČŠąį─ŻöMĮY║Ž░l╣Ō╝ÜŠ·ČŠąįīŹ“×ĮY╣¹▒Ē├„▓┐Ęųųąķg«a╬’Ģ■ī¦ų┬╝▒ąįČŠąįĄ─╔Ž╔²Ż¼▀@ŅÉųąķg«a╬’▀Mę╗▓ĮĘųĮŌ×ķąĪĘųūė¤oÖC╬’║¾ČŠąįĢ■ĮĄĄ═Ż¼║¾└mĄ─īŹ“×┼cæ¬ė├┐╔ęįčėķLĘ┤æ¬ĢrķgęįĮĄĄ═╚▄ę║ČŠąįĪŻŻ©üĒį┤Ż║ÅBķT└Ē╣żīWį║╦«┘Yį┤ŁhŠ│蹊┐╦∙Ż¼šŃĮŁ╣żśI┤¾īW═┴─Š╣ż│╠īWį║Ż¼ÅBķT╩ą╦«┘Yį┤└¹ė├┼c▒Żūoųž³cīŹ“×╩꯮



