╬█─Ó╬³┴ūĘĮ╩ĮĄ─▐D╗»
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2017-1-9 11:03:24
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪĄ¬Īó ┴ūĄ─▀^┴┐┼┼Ę┼╩Ūę²Ų╦«¾wĖ╗ĀIB╗»Ą─ų„ę¬įŁę“. é„Įy╔·╬’ĀIB╬’╚ź│²ŽĄĮyųąŻ¼Ą¬Ą─╚ź│²═©▀^ā╔éĆļAČ╬═Ļ│╔Ż¼╝┤║├觎§╗»║═╚▒č§Ę┤Ž§╗»Ż¼Č°┴ūĄ─╚ź│²ät╩Ū└¹ė├Š█┴ū╬ó╔·╬’Ą─ģÆč§ßī┴ū╝░║├č§(╗“╚▒č§)│¼┴┐╬³┴ū╠žąįį┌Į╗╠µģÆč§/║├č§▀\ąąŁhŠ│Ž┬īŹ¼F[1, 2, 3, 4].
ĪĪĪĪī”ė┌┐╔īŹ¼F═¼▓Į├ōĄ¬│²┴ū╣”─▄Ą─╬█╦«╠Ä└ĒÅS╣ż╦ćŻ¼Ž§╗»║═║├č§╬³┴ū═©│Żį┌═¼ę╗éĆĘ┤æ¬│žųą▀Mąą. ├ōĄ¬▀^│╠Ą─ųąķg«a╬’Ī¬Ī¬ü厧╦ß¹}Ż¼į┌Ž§╗»║═Ę┤Ž§╗»▀^│╠ųąŠ∙Ģ■«a╔·. į┌«öĮ±─▄į┤╬ŻÖC╝░│½ī¦Ą═╠╝╣Ø─▄╝╝ągĄ─Ģr┤·▒│Š░Ž┬Ż¼Č╠│╠├ōĄ¬╣ż╦ćę“Ųõ╠Ä└Ēą¦┬╩Ė▀Īó ─▄į┤Ž¹║─Ą═╝░╬█─Ó«a┴┐╔┘Ą╚ā׳c╩▄ĄĮ▒ŖČÓ蹊┐š▀║═╬█╦«ÅS▀\ĀI╣▄└Ēš▀ŪÓ▓AŻ¼▓╔ė├Č╠│╠├ōĄ¬╝╝ąg▒ŃęŌ╬Čų°║├č§▀^│╠ųąėąĖ³ČÓ┴┐ü厧╦ß¹}Ą─Ęe└█. Į³Äū─ĻŻ¼ĻPė┌ü厧╦ß¹}ī”╬█╦«╔·╬’╠Ä└ĒŽĄĮyĖ„Š·╚║ęųųŲ╠žąįĄ─蹊┐ŅHČÓ[5, 6, 7, 8, 9, 10, 11]Ż¼Ųõųąęį░─┤¾└¹üå└ź╩┐╠m┤¾īWYuan ZhiguoĮ╠╩┌šnŅ}ĮMĄ─蹊┐ūŅ×ķ╔Ņ╚ļŻ¼Ųõ蹊┐ĮY╣¹▒Ē├„Ż¼╬█╦«├ōĄ¬│²┴ūŽĄĮyā╚Ą─šµš²ęųųŲä®╩Ūü厧╦ß¹}Ą─┘|ūė╗»«a╬’Ī¬Ī¬ė╬ļxü厧╦ß(Č°ĘŪü厧╦ß¹}▒Š╔Ē[12, 13, 14, 15, 16, 17, 18, 19, 20]. Įžų┴─┐Ū░Ż¼ĻPė┌FNAĄ─蹊┐ų„ę¬░³└©ī”░▒č§╗»╝ÜŠ·Īó ü厧╦ß¹}č§╗»Š·Īó Ę┤Ž§╗»╝ÜŠ·╝░Š█┴ūŠ·Ą╚╬ó╔·╬’į÷ų│┼c«a─▄Ą─ęųųŲū„ė├[14, 15, 16, 17, 18, 19, 20, 21, 22, 23]. ╚╗Č°Ż¼╔Ž╩÷蹊┐┤¾ČÓ▓╔ė├┼·╩Įįć“ׯ¼ĻPė┌FNAķLŲ┌ęųųŲū„ė├Ą─蹊┐§rėął¾Ą└. īŹ“×╩ę蹊┐║═īŹļH╬█╦«╠Ä└ĒÅS▀\ĀIĮø“×’@╩ŠŻ¼įŁėąĄ─╔·╬’ĀIB╬’╚ź│²╣ż╦ćśOęūå╩╩¦Ųõ│²┴ū╣”─▄Ż¼┤╦═ŌŻ¼ī”īŹ¼FČ╠│╠├ōĄ¬Ą─╬█╦«╠Ä└ĒÅSĄ─š{▓ķ░l¼FŻ¼║├č§Č╬ü厧╦ß¹}Ęe└█┴┐╗∙▒ŠŠS│ųį┌20 mg ĪżL-1ęįā╚Ż¼ę“┤╦Ż¼┐╝▓ņįōØŌČ╚ĘČć·ā╚Ą─ü厧╦ß¹}╝░ŽÓæ¬ØŌČ╚Ą─FNAī”║├č§╬³┴ūŽĄĮyĄ─ķLŲ┌ęųųŲū„ė├ė╚×ķ▒žę¬.
ĪĪĪĪ▒ŠčąŠ┐▓╔ė├Į╗╠µģÆč§/║├č§SBRĘ┤æ¬Ų„Ż¼į┌£žČ╚×ķ21-23ĪµĄ─Śl╝■Ž┬åóäėįō├ōĄ¬│²┴ūŽĄĮy▓óŽ“ŽĄĮyā╚ķLŲ┌═Č╝ėü厧╦ß¹}Ż¼ęį┐╝▓ņFNAī”║├č§╬³┴ūąį─▄Ą─ķLŲ┌ęųųŲū„ė├╝░±Z╗»║¾╬█─Ó╬³┴ūĘĮ╩ĮĄ─▐D╗».
ĪĪĪĪ1 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ1.1 įć“×čbų├╝░▀\ąą
ĪĪĪĪSBRĘ┤æ¬Ų„ė╔ėąÖC▓Ż┴¦ųŲ│╔Ż¼╔Ž▓┐×ķłAų∙ą╬Ż¼Ąū▓┐×ķłAÕF¾wŻ¼┐éėąą¦╚▌Ęe5.4 L. Ę┤æ¬Ų„▒┌┤╣ų▒ĘĮŽ“įOų├ę╗┼┼ķgŠÓ10 cmĄ─╚Īśė┐┌Ż¼ė├ė┌╚Īśė║═┼┼╦«Ż¼Ąū▓┐įOėą┼┼─Ó┐┌; ŲžÜŌ▓╔ė├┐šÜŌē║┐sÖCŻ¼ÜŌ┴┐ė╔▐Dūė┴„┴┐ėŗš{╣ØŻ¼ż╔░ēKŲžÜŌŅ^ė├ęįŽ“╗ņ║Žę║é„▀fč§ÜŌ; Ę┤æ¬Ų„▀M/│÷╦«Īó öć░ĶĪó ŲžÜŌ╝░▀\ąąļAČ╬Ą─pHųĄš{╣ØŠ∙▓╔ė├ĦėąLabview▄ø╝■ŠÄ│╠Ą─ėŗ╦ŃÖCŽĄĮy╝ėęį┐žųŲŻ¼įć“×čbų├╚ńłD 1╦∙╩Š.
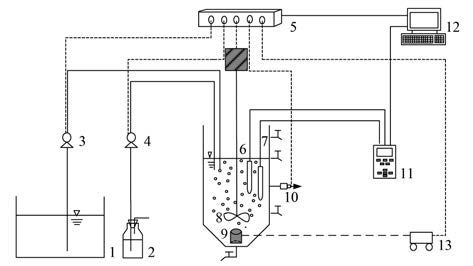
ĪĪĪĪłD 1 SBR╔·╬’│²┴ūĘ┤æ¬Ų„╩ŠęŌ
ĪĪĪĪ1. ╦«Žõ; 2. HCl╚▄ę║; 3. ╚õäė▒├; 4. ┴„┴┐ą═╚õäė▒├; 5. pH┐žųŲŽĄĮy; 6. pH╠ĮŅ^; 7. DO╠ĮŅ^; 8. öć░Ķčbų├; 9. ż╔│ēKŲžÜŌŅ^; 10. ļŖ┤┼ķy; 11. Multi 3420į┌ŠĆ£yČ©āx; 12. ėŗ╦ŃÖC; 13. ┐šÜŌē║┐sÖC
ĪĪĪĪĘ┤æ¬Ų„├┐╠ņ▀\ąą3éĆų▄Ų┌Ż¼├┐ų▄Ų┌8 hŻ¼░³└©2 hģÆ觯¼5 h║├č§╝░1 h│┴ĄĒĪó ┼┼╦«Īó ķeų├Ż¼įć“×┐é╣▓▀Mąą178 dŻ¼Ęų×ķ6éĆ╣żørŻ¼Ė„╣żørį┌ģÆč§ĮY╩°Ż¼╝┤║├č§│§╩╝ļAČ╬╦▓Ģr═Č╝ė▓╗═¼┴┐ü厧╦ßŌcØŌ┐sę║Ż¼╩╣╗ņ║Žę║ā╚NO2--NØŌČ╚Ęųäe×ķ0Īó 2Īó 5Īó 10Īó 15Īó 20 mg ĪżL-1Ż¼ŽÓæ¬Ą─FNAØŌČ╚ė╔╣½╩ĮŻ║
ĪĪĪĪėŗ╦Ń╦∙Ą├. Ę┤æ¬Ų„┼┼╦«▒╚×ķ1/3Ż¼£žČ╚▒Ż│ųį┌21-23ĪµŻ¼pHųĄŠS│ųį┌6.9-7.5ų«ķgŻ¼╬█─Ó²g×ķ10 d.
ĪĪĪĪ╚▒č§╬³┴ūąĪįćŻ║ Ęųäeė┌įć“×Ė„╣żørĄ─ĘĆČ©▀\ąąŲ┌ķg▀MąąŻ¼ģÆč§ĮY╩°║¾ė┌SBRĘ┤æ¬Ų„╚Ī─Ó╦«╗ņ║Žę║ų├ė┌2 LĘ┤æ¬Ų┐ųą╝ėļŖĮŌ┘|╚▄ę║Ž┤─ÓŻ¼╚▒č§Č╬│§╩╝╦▓Ģr═Č╝ė┴ū(PO43--P=20 mg ĪżL-1)║═ļŖūė╩▄¾w(NO2--N╗“NO3--N 10mg ĪżL-1)Ż¼Ę┤æ¬╣▓▀Mąą5 hŻ¼Ųõ╦¹Śl╝■═¼─ĖĘ┤æ¬Ų„.
ĪĪĪĪ1.2 įć“×╦«┘|╝░ĮėĘN╬█─Ó
ĪĪĪĪįć“×ė├─ŻöMÅU╦«ė╔╠╝į┤ę║Īó ┴ūę║Īó ØŌ┐sę║╝░╬ó┴┐į¬╦ž┼õųŲČ°│╔. ╠╝į┤ę║ė╔ęę╦ßŌc┼õųŲČ°│╔Ż¼┴ūę║ė╔ KH2PO4┼õųŲČ°│╔Ż¼Ųõųą╚▄ĮŌąįš²┴ū╦ß¹}(PO43--P)┘|┴┐ØŌČ╚×ķ4 g ĪżL-1. ØŌ┐sę║(1 L)ė╔53.5 g NH4ClŻ¼45 g MgSO4 Īż7H2OŻ¼18 g KClĮM│╔Ż¼╬ó┴┐į¬╦žę║[27](1L)ė╔5.51 gÖÄ├╩╦߯¼4.03 g▒Į╝ū§Ż░Ę╗∙§ź╦߯¼3.03 g FeCl3 Īż6H2OŻ¼0.5 g H3BO3Ż¼0.12 g CuSO4 Īż5H2OŻ¼0.06 g KIŻ¼0.24 g MnCl2 Īż4H2OŻ¼0.06 g NaMoO4 Īż2H2OŻ¼0.3 g ZnSO4 Īż7H2OŻ¼0.06 g CoCl Īż6H2OŻ¼10 g EDTAŻ¼0.06 g NaMoO4 Īż2H2OŻ¼0.06 g NiCl2 Īż6H2OĮM│╔. 1 L─ŻöMÅU╦«╝ė╚ļ┴ūę║2 mLŻ¼╠╝į┤ę║ęę╦ßŌc6.08 g╚▄ė┌╦«ųąĪó ØŌ┐sę║1 mL╝░╬ó┴┐į¬╦žę║1 mLŻ¼ė╔┤╦Ą├│÷Ż¼▀M╦«ųąų„ę¬╬█╚Š╬’×ķCOD 400(1-138 d)╗“550 mg ĪżL-1(138-178 d)Ż¼PO43--P 8 mg ĪżL-1Ż¼NH4+-N 14 mg ĪżL-1.
ĪĪĪĪĮėĘN╬█─Ó╚ĪūįĖ╩├C╩Ī╠mų▌╩ąŲ▀└’║ėģ^╬█╦«╠Ä└ĒÅS4╠¢ŲžÜŌ│žŻ¼įō╬█╦«ÅS╬█─ÓŠ▀ėąę╗Č©├ōĄ¬│²┴ūąį─▄Ż¼╬█─ÓĖ„ĒŚųĖś╦ąį─▄┴╝║├.
ĪĪĪĪ1.3 Ęų╬÷ĒŚ─┐╝░ĘĮĘ©
ĪĪĪĪ╦«┘|Ęų╬÷ĒŚ─┐ųąŻ¼COD▓╔ė├COD┐ņ╦┘£yČ©āx£yČ©Ż¼PO43--P▓╔ė├ŃfõR┐╣Ęų╣Ō╣ŌČ╚Ę©£yČ©Ż¼NH4+-N▓╔ė├╝{╩Žįćä®Ęų╣Ō╣ŌČ╚Ę©£yČ©Ż¼NO2--N▓╔ė├N-(1▌┴╗∙)-ęęČ■░ĘĘų╣Ō╣ŌČ╚Ę©£yČ©Ż¼NO3--N▓╔ė├„ĻŽŃ▓▌ĘėĘų╣Ō╣ŌČ╚Ę©£yČ©Ż¼MLSSŻ¼MLVSS▓╔ė├×V╝łųž┴┐Ę©£yČ©Ż¼SV▓╔ė├30 min│┴ĮĄĘ©£yČ©. £žČ╚Īó pHųĄ║═╚▄ĮŌč§£yČ©▓╔ė├Ą┬ć°Multi 3420į┌ŠĆ£yČ©āxį┌ŠĆ▒O£y.
ĪĪĪĪ2 ĮY╣¹┼cėæšō
ĪĪĪĪ2.1 ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮyĄ─╬█╚Š╬’╚ź│²ąį─▄
ĪĪĪĪĘ┤æ¬Ų„▀\ąąŲ┌ķgŻ¼Öz£y░l¼F│÷╦«CODØŌČ╚Š∙Ą═ė┌10 mg ĪżL-1Ż¼▀M╦«ųą95%ęį╔ŽCOD▒╗╚ź│²Ż¼šf├„▒ŠčąŠ┐▓╔ė├Ą─FNAØŌČ╚ī”CODĮĄĮŌø]ėąė░Ēæ.
ĪĪĪĪłD 2×ķĖ„╣żørŚl╝■Ž┬Ż¼═Č╝ė▓╗═¼ØŌČ╚ü厧╦ß¹}║¾Ę┤æ¬Ų„│÷╦«Ė„ą╬æBĄ¬╝░┐饬Ą─╚ź│²Ūķør. Å─ųą┐╔ų¬Ż¼į┌Ę┤æ¬Ų„▀\ąąĄ─178 dā╚Ż¼│÷╦«NH4+-N╩╝ĮK╬┤Öz│÷Ż¼╚ź│²┬╩▀_100%; ī”Ė„▀\ąą╣żørĄ─ų▄Ų┌▒O£yę▓’@╩ŠŻ¼NH4+-Nį┌60 minŠ∙ęčÅžĄūĮĄĮŌ(╬┤Įo│÷)Ż¼šf├„▒ŠčąŠ┐▓╔ė├Ą─FNAØŌČ╚ī”NH4+-NĄ─╚ź│²ø]ėąė░ĒæŻ¼ī”▒╚░l¼FŻ¼▒ŠčąŠ┐FNAūŅĖ▀ØŌČ╚(ęįHNO2-NėŗŻ¼Ž┬═¼)×ķ1.94Ī┴10-3 mg ĪżL-1Ż¼┼cęčėął¾Ą└Ą─AOB╗Ņąį╩▄ęųųŲ│╠Č╚×ķ50%Ģrī”æ¬Ą─FNAØŌČ╚ŽÓ▓ŅĮ³100▒Č[14]Ż¼▀Mę╗▓ĮūC├„│ŻęÄ╬█╦«╠Ä└ĒÅSė╔ü厧╦ß¹}Ęe└█╦∙Ą├FNAī”AOBĄ─į÷ų│┼c«a─▄┤·ųx╗Ņäėė░Ēæ╔§╬ó. ┤╦═ŌŻ¼ü厧╦ß¹}═Č╝ė┴┐×ķ0-15 mg ĪżL-1ĘČć·ā╚Ż¼ŽĄĮy│÷╦«ųąÜł┴¶Ą─NO2--N┴┐Š∙ąĪė┌0.1 mg ĪżL-1Ż¼│÷╦«NO3--NĘe└█┴┐ätļSų°║├č§│§╩╝ļAČ╬NO2--N═Č┴┐Ą─╝ė┤¾Č°į÷ČÓŻ¼ūŅĖ▀═Č╝ė┴┐ī”æ¬Ą─ŲĮŠ∙ųĄ×ķ5.11 mg ĪżL-1Ż¼┐饬ōp╩¦┬╩ę╗ų▒▒Ż│ųŲĮĘĆŻ¼Š∙Ė▀ė┌80%. ü厧╦ß¹}═Č┴┐╠ß╔²ų┴20 mg ĪżL-1║¾Ż¼│÷╦«ų▓Į│÷¼FNO2--NĄ─Ęe└█Ż¼ŲĮŠ∙ųĄ▀_4.75 mg ĪżL-1Ż¼NO3--NŲĮŠ∙Ęe└█┴┐ę▓╔²ų┴9.77 mg ĪżL-1Ż¼┐饬ōp╩¦┬╩āH×ķ56.88%.
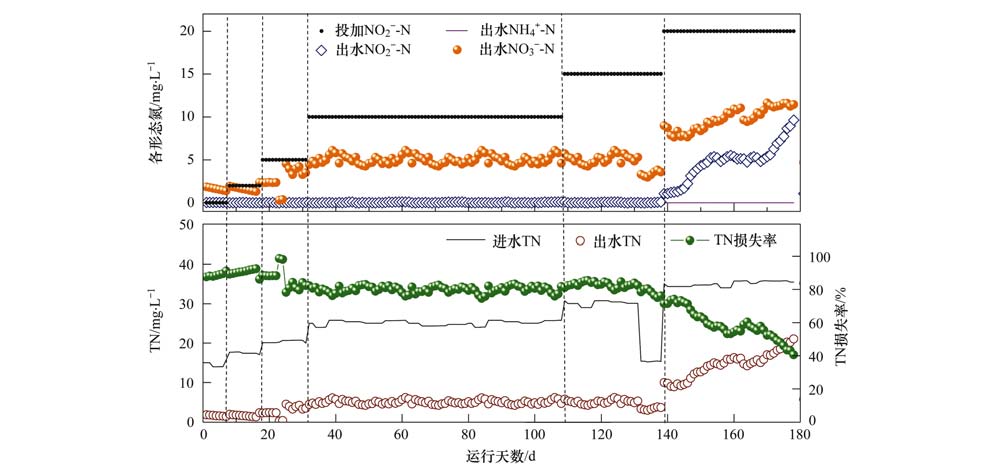
ĪĪĪĪłD 2 ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮy│÷╦«Ė„ą╬æBĄ¬╝░┐饬╚ź│²Ūķør
ĪĪĪĪ▒Ē 1┴ą│÷┴╦▓╗═¼FNAØŌČ╚Ž┬║├č§ļAČ╬Ą¬Ą─▐D╗»Ūķør. Å─ųą┐╔ęį┐┤│÷Ż¼Ė„╣żørŽ┬Ż¼║├č§│§╩╝ļAČ╬═Č╝ėĄ─NO2--Nōp╩¦┴┐ė╔╬┤═Č╝ėĢrĄ─0 mg ĪżL-1ųØu╔²ų┴═Č╝ė15 mg ĪżL-1ĢrĄ─11.495 mg ĪżL-1. įć“ץ─Ą┌132-138 dŻ¼│ĘõN▀M╦«ųąĄ─NH4+-NŻ¼ĮY║ŽłD 2░l¼FŻ¼║├č§Č╬═Č╝ėĄ─15 mg ĪżL-1 NO2--N▐D╗»×ķ│÷╦«NO3--NĄ─┴┐āHėą3.382 mg ĪżL-1Ż¼įōĢrķgČ╬═¼▒Š╣żør╬┤│ĘõN▀M╦«NH4+-NĄ─NO3--NĘe└█┴┐▓ŅųĄ×ķ1.725 mg ĪżL-1Ż¼▀@┼cNO2--N═Č┴┐×ķ0 mg ĪżL-1ĢrŻ¼╝┤▀M╚ļ¾wŽĄā╚Ą─Ą¬āHė╔▀M╦«NH4+-N╠ß╣®ĢrĄ─NO3--NĘe└█┴┐(1.617 mg ĪżL-1)ŽÓ«ö. ═¼ĢrŻ¼ī”Ė„╣żørŽ┬╗ņ║Žę║╚▄ĮŌ觥─į┌ŠĆ▒O£y’@╩ŠŻ¼▀M╚ļ║├č§ļAČ╬║¾Ż¼╚▄ĮŌč§į┌30 minā╚Š∙┐ņ╦┘╔²ų┴2 mg ĪżL-1ęį╔ŽŻ¼įōŁhŠ│▓ó▓╗└¹ė┌═¼▓ĮŽ§╗»Ę┤Ž§╗»ū„ė├Ż¼Č°Ūę┤╦║¾¾wŽĄā╚NO2--NØŌČ╚╚į▒Ż│ųŽ┬ĮĄ┌ģä▌Ż¼NO3--NØŌČ╚ģs┌ģė┌ŲĮĘĆŻ¼šf├„NO3--NĄ─▐D╗»į┌║├č§ļAČ╬Ą─Ū░30 minā╚ęč╗∙▒Š═Ļ│╔Ż¼║¾270 minā╚NO2--N▓óĘŪ▒╗NOB└¹ė├Ż¼ŲõŽ¹║─┐╔─▄ė╔Ųõ╦¹Š·ĘN═Ļ│╔Ż¼▀@ę╗¼FŽ¾┼cPijuanĄ╚Ą─蹊┐ę╗ų┬[17]. ▀ĆųĄĄ├ę╗╠ߥ─╩ŪŻ¼║├č§ļAČ╬30 min║¾╗ņ║Žę║ųąNO2--N┼cPO43--PØŌČ╚═¼ĢrŽ┬ĮĄŻ¼▒Ŗ╦∙ų▄ų¬Ż¼│²O2═ŌNO2--N║═NO3--Nę▓─▄▒╗PAOs└¹ė├Ż¼▓╗═¼Ą─╩ŪNO2--N║═NO3--Nū„×ķļŖūė╩▄¾wė├ęį╬³┴ūį┌╚▒觌l╝■Ž┬▀MąąŻ¼ę“┤╦Ż¼╚ń╣¹╝┘įOėąO2║═NO2--Nā╔ĘNļŖūė╩▄¾w═¼Ģr┤µį┌Ą─ŪķørŽ┬Ż¼┼┼│²PAOs└¹ė├▓╗═¼ļŖūė╩▄¾w╬³┴ūĄ─«a─▄▓Ņ«ÉŻ¼NO2--N║═O2ī”PAOsŠ▀ėąŽÓ═¼ĖéĀÄ┴”Ż¼ę“Č°Ż¼NO2--Nį┌║├觌l╝■Ž┬═¼śė─▄▒╗PAOs└¹ė├Ż¼▀@▓┼║Ž└ĒĮŌßī┴╦NO2--Nį┌║├č§Č╬┤¾┴┐ōp╩¦▀@ę╗¼FŽ¾.
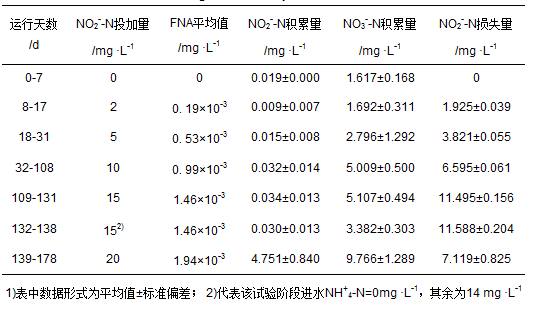
ĪĪĪĪ▒Ē 1 ▓╗═¼FNAŚl╝■Ž┬║├č§ļAČ╬Ą¬Ą─▐D╗»┴┐1)
ĪĪĪĪłD 3×ķ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮy▀MĪó │÷╦«║═ģÆč§─®Ų┌Ą─PO43--PØŌČ╚╝░Ųõ╚ź│²┬╩. Å─ųą┐╔ęŖŻ¼│²═Č╝ė20 mg ĪżL-1 NO2--NĄ─Ū░30 d═ŌŻ¼═Č╝ėNO2--N║¾ŽĄĮyģÆč§─®Ų┌┴ūØŌČ╚ŲĮŠ∙Ė▀ė┌═Č╝ėŪ░. ▒ŠčąŠ┐ųąNO2--N═Č╝ė┴┐<5 mg ĪżL-1Ż¼╝┤š█║ŽFNAØŌČ╚Ą═ė┌0.53Ī┴10-3 mg ĪżL-1ĢrŻ¼ŽĄĮyĄ─│÷╦«PO43--PØŌČ╚ļmėąąĪĘ∙▓©äėĄ½║▄┐ņ─▄┌ģė┌ĘĆČ©Ż¼│²┴ū┬╩▒Ż│ųį┌95%ęį╔ŽŻ¼│÷╦«ØŌČ╚Ą═ė┌0.5 mg ĪżL-1. ▀Mę╗▓Į╠ßĖ▀FNAØŌČ╚ų┴0.99Ī┴10-3 mg ĪżL-1║¾Ż¼ŽĄĮy│²┴ūąį─▄čĖ╦┘É║╗»Ż¼│÷╦«┴ūØŌČ╚ć└ųž│¼ś╦Ż¼į┌Ė─ūāFNAØŌČ╚Ą─Ū░4 dā╚Ż¼┴ūÄū║§¤o╚ź│²Ż¼┤╦║¾ė╔ė┌ŽĄĮyųąPAOsī”FNAĄ─▀mæ¬─▄┴”ų▓Įį÷ÅŖŻ¼╬█─Ó│²┴ūąįųØu╗ųÅ═Ż¼Ą½╗ųÅ═╦∙ąĶĢrķg▌^ķLŻ¼50 d║¾│²┴ū┬╩ŲĮŠ∙╗ųÅ═ų┴64.42%Ż¼ūŅĖ▀71.1%. ╔Ž╩÷FNAØŌČ╚ī”æ¬Ą─╬³┴ūąį─▄╩▄ęųųŲ│╠Č╚├„’@Ą═ė┌╬─½Ił¾Ą└Ą─FNA┼RĮńØŌČ╚Ęųäe×ķ0.000 5 mg ĪżL-1║═0.001 mg ĪżL-1Ģr╦∙ī”æ¬Ą─╬³┴ūąį─▄╩▄ęųųŲ│╠Č╚50%║═75%[17]. ęį╔ŽĘų╬÷▒Ē├„Ż¼FNAī”PAOs║├č§╬³┴ū─▄┴”Ą─▓╗└¹ė░Ēæ┐╔═©▀^ķLŲ┌▀\ąąų▓Į╗ųÅ═Ż¼Ą½▓╗─▄═Ļ╚½╗ųÅ═. į┌┤╦Ų┌ķgĄ──│éĆų▄Ų┌ā╚Ż¼│ĘõNFNA═Č╝ėįć“×░l¼FŻ¼ŽĄĮyĄ─│²┴ū─▄┴”ėąę╗Č©│╠Č╚Ą─╠ßĖ▀Ż¼šf├„FNAī”║├č§╬³┴ūąį─▄Ą─ęųųŲ╩Ū┐╔─µĄ─. į÷┤¾NO2--N═Č┴┐ų┴15 mg ĪżL-1Ż¼╝┤FNA×ķ1.46Ī┴10-3 mg ĪżL-1Ż¼│÷╦«┴ūØŌČ╚į┌Ė─ūā╣żør║¾į┘┤╬│÷¼F┤¾Ę∙Ž┬ĮĄŻ¼Ą½ī”▒╚╔Žę╗éĆ╣żørŻ¼▓©äėĄ─Ę∙Č╚ėą╦∙£pąĪ. Ęų╬÷šJ×ķŻ¼ė╔ė┌ķLŲ┌═Č╝ėNO2--NĄ─±Z╗»ą¦æ¬╩╣Ą├PAOsī”FNAĄ─▀mæ¬─▄┴”į÷ÅŖŻ¼įō╣żørā╚Įø▀^12 d▀\ąąŽĄĮy│²┴ū┬╩ŲĮŠ∙╗ųÅ═ų┴67.33%Ż¼▌^Ū░ę╗╣żørĄ─╗ųÅ═▀^│╠┤¾×ķ┐sČ╠. į┘┤╬╠ßĖ▀FNAØŌČ╚ų┴1.94Ī┴10-3 mg ĪżL-1Ż¼│²┴ū┬╩į┘Č╚┤¾Ę∙▓©äėŻ¼į┌įō╣żørĄ─Ū░10 dā╚Ż¼│÷╦«PO43--PØŌČ╚ėąĢr╔§ų┴Ė▀ė┌▀M╦«ØŌČ╚Ż¼ų«║¾Ż¼│²┴ū┬╩Įø▀^20 dų▓Į╗ųÅ═ĄĮ44.14%.
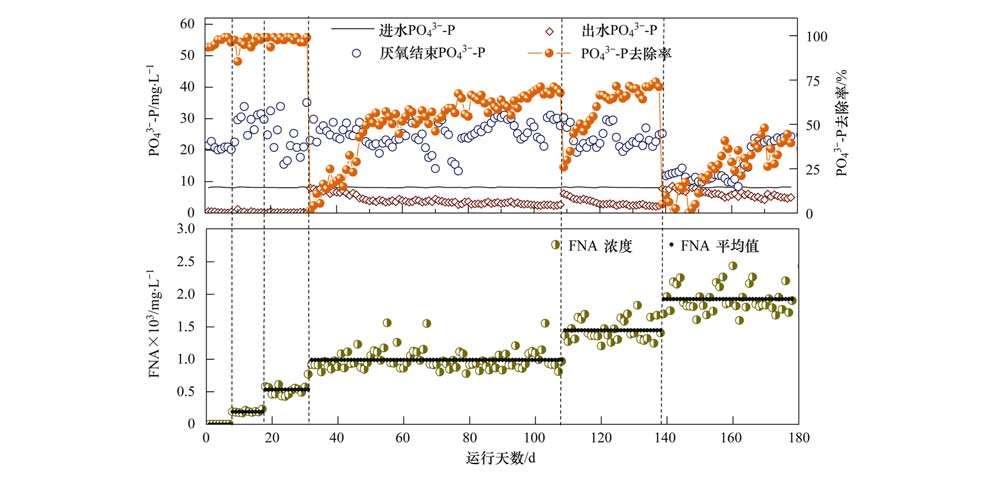
ĪĪĪĪłD 3 ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮyĖ„ļAČ╬┴ūØŌČ╚╝░Ųõ╚ź│²┬╩
ĪĪĪĪė╔ė┌ūŅ║¾ę╗éĆ╣żør│÷╦«ųą┤µį┌┤¾┴┐NO2--N║═NO3--NĘe└█(łD 2)Ż¼įć“×║¾Ų┌▀Ćį°╠ßĖ▀▀M╦«CODØŌČ╚ų┴550 mg ĪżL-1ęįŲ┌╝ėÅŖĘ┤Ž§╗»Å─Č°Ė─╔ŲŽĄĮy│²┴ūąį─▄(╬┤Įo│÷)Ż¼Įø▀^Į³40 dĄ─▀\ąąįōļAČ╬│÷╦«NO2--N║═NO3--NĘe└█┴┐ų▓ĮŽ┬ĮĄų┴0.30 mg ĪżL-1║═4.62 mg ĪżL-1Ż¼Č°ģÆč§─®Ų┌PO43--PØŌČ╚ätį┌╠ßĖ▀╠╝į┤┴┐║¾╝┤┐╠ė╔įŁüĒĄ─24.45 mg ĪżL-1┤¾Ę∙╔Ž╔²ų┴55 mg ĪżL-1ū¾ėęŻ¼║├č§╬³┴ū┴┐ęÓė╔17.71 mg ĪżL-1╠ßĖ▀ų┴45.51 mg ĪżL-1Ż¼▒M╣▄╚ń┤╦Ż¼ī”│÷╦«PO43--PĄ─▒O£yģs░l¼FŲõ╚ź│²┬╩▓╗╔²Ę┤ĮĄŻ¼ļS║¾ŠÅ┬²╗ųÅ═ų┴25%ū¾ėę. Ęų╬÷šJ×ķŻ¼╠ßĖ▀COD┐╔£pŠÅPAOs┼c«ÉBĘ┤Ž§╗»Š·ī”╠╝į┤Ą─ĀÄŖZŻ¼Č°ė╔┤╦╠ßĖ▀Ą─ßī┴ū┴┐ī¦ų┬Š█┴ūŠ·╬³┴ūžō║╔į÷┤¾Ż¼Å─Č°ę²Ų│²┴ū┬╩ę“╬³┴ūĢrķg▓╗ūŃČ°Ž┬ĮĄĄ─¼FŽ¾Ż¼Ą½ßī┴ū┴┐║═╬³┴ū┴┐Ą─į÷┤¾Ż¼╝┤PAOsĄ─▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩Š∙╠ßĖ▀ų┴╬┤į÷╝ė╠╝į┤┴┐Ą─2▒Čęį╔ŽŻ¼Ę┤ė││÷╠ßĖ▀▀M╦«╠╝į┤ėąų·ė┌ŠÅĮŌFNAī”║├č§╬³┴ūĄ─ęųųŲ.
ĪĪĪĪ2.2 ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮyĄõą═ų▄Ų┌ā╚╬█╚Š╬’Ą─ūā╗»ęÄ┬╔
ĪĪĪĪłD 4×ķ▓╗═¼╣żørŽ┬ŽĄĮyĄõą═ų▄Ų┌ā╚PO43--P║═Ė„ą╬æBĄ¬╝░DOĄ─ØŌČ╚ūā╗»ęÄ┬╔. Å─ųą┐╔ų¬Ż¼įć“×▀MąąĄ─6éĆ╣żørā╚Š∙ėąßī┴ū║═╬³┴ū¼FŽ¾ŪęūŅ┤¾ßī┴ūØŌČ╚│÷¼Fį┌ģÆč§ĮY╩°Ģr┐╠. į┌Ė„╣żørģÆč§ĢrČ╬ā╚Ż¼DOØŌČ╚ŠS│ųį┌śOĄ═ĘČć·Ż¼╝┤0.02 mg ĪżL-1ū¾ėęŻ¼PAOsīó¾wā╚Š█┴ūęįš²┴ū╦ß¹}Ą─ą╬╩ĮßīĘ┼│÷üĒ▓ó«a╔·─▄┴┐Ż¼▀MČ°└¹ė├įō─▄┴┐╬³╩š╗ņ║Žę║ųąĄ─ō]░ląįų¼ĘŠ╦ß(VFAs)▓óęįŠ█┴u╗∙ų¼ĘŠ╦ß(PHAs)Ą─ą╬╩Į┘A┤µį┌¾wā╚; į┌┤╦Ų┌ķgŻ¼NH4+-NØŌČ╚ė╔ė┌╗Ņąį╬█─ÓĄ─╬³ĖĮū„ė├ėąąĪĘ∙ĮĄĄ═(<1 mg ĪżL-1). ║├č§ĢrČ╬ā╚Ż¼DOØŌČ╚Å─0.02 mg ĪżL-1┐ņ╦┘╔²ų┴2 mg ĪżL-1ęį╔ŽŻ¼PAOsęįĮĄĮŌPHAs×ķ─▄┴┐üĒį┤īŹ¼F╬ó╔·╬’╔·ķLĪó ╠ŪįŁ║Ž│╔ęį╝░┴ūĄ─▀^┴┐╬³╩š; NH4+-N▒╗┐ņ╦┘ĮĄĮŌ▐D╗»×ķNO2--NŻ¼▓óūŅĮK▐D╗»×ķNO3--N. ╣żør1ųąŻ¼╝┤ŽĄĮyĄ─åóäėļAČ╬Ż¼ģÆč§Č╬ĮY╩°ĢrĄ─┴ūØŌČ╚×ķ25.14 mg ĪżL-1; NH4+-NŠS│ųį┌3.35 mg ĪżL-1ęį╔Ž. ║├č§ļAČ╬Ż¼DOØŌČ╚┐ņ╦┘╔²Ė▀▓óŠS│ųį┌4-6 mg ĪżL-1ų«ķgŻ¼PAOsį┌Ę┤æ¬Ģrķgā╚═Ļ│╔╬³┴ū▀^│╠Ż¼│÷╦«<0.5 mg ĪżL-1; NH4+-Nį┌ėąč§Śl╝■Ž┬┐ņ╦┘ĮĄĮŌŻ¼Ę┤æ¬─®Č╦│÷¼F1.617 mg ĪżL-1Ą─NO3--NĘe└█. ╣żør2ųąŻ¼▒M╣▄į┌ģÆč§Č╬ĮY╩°Ģr┐╠Ž“ŽĄĮyā╚═Č╝ėØŌČ╚×ķ2 mg ĪżL-1Ą─NO2--NŻ¼Ą½ģÆč§ßī┴ū┴┐▌^╣żør1ėą┤¾Ę∙╔²Ė▀Ż¼┴ūØŌČ╚▀_42.78 mg ĪżL-1. Ęų╬÷šJ×ķŻ¼ė╔ė┌FNAĄ─ĮŌ±Ņ┬ōū„ė├Ż¼PAOs▒žĒÜ╠ßĖ▀║¶╬³╦┘┬╩Ż¼╝┤ĘųĮŌĖ³ČÓĄ─Š█┴ū(Poly-P)ęį▒├│÷Ė³ČÓ┘|ūėÅ─Č°ŠS│ų┘|ūė“īäė┴”(PMF)Ą─║ŃČ©. 蹊┐▀Ć░l¼FŻ¼ė╔ė┌ßī┴ū┴┐Ą─╠ßĖ▀ī¦ų┬PAOsį┌║├č§Č╬Ą─žō║╔į÷┤¾Ż¼Ą½╬³┴ū▀^│╠į┌Ę┤æ¬Ģrķgā╚╚į─▄ÅžĄū═Ļ│╔Ż¼šf├„PAOsĄ─╬³┴ū─▄┴”ėą╦∙╠ßĖ▀; ī”║├č§│§╩╝ļAČ╬Ž“ŽĄĮy═Č╝ėĄ─NO2--NØŌČ╚£yČ©╝░öĄō■Ęų╬÷░l¼FŻ¼NO2--N═Č╝ė┐é┴┐│÷¼F95%ęį╔ŽĄ─ōp╩¦Ż¼āHėą╩ŻėÓę╗ąĪ▓┐Ęų▐D╗»×ķNO3--NŻ¼šf├„NO2--Nį┌║├č§ļAČ╬▒╗│²ü厧╦ß¹}č§╗»Š·(NOB)ęį═ŌĄ─Ųõ╦¹╬ó╔·╬’╦∙Ž¹║─Ż¼Ą½Š▀¾w▒╗──ĘN╬ó╔·╬’Š·╚║└¹ė├╝░ŲõĮĄĮŌÖCųŲ╚į▓╗├„┤_. ╣żør3ųąŻ¼NO2--NĄ─═Č╝ė┴┐╠ßĖ▀ų┴5 mg ĪżL-1Ż¼│²┴ū┬╩╚įĮėĮ³100%Ż¼šf├„FNAØŌČ╚Ą═ė┌0.53Ī┴10-3 mg ĪżL-1ĢrŻ¼ŽĄĮyĄ─│²┴ūąį─▄╬┤╩▄ęųųŲ. ╣żør4Ż¼╝┤NO2--N═Č╝ė┴┐×ķ10 mg ĪżL-1Ż¼ōQ╦Ń×ķFNAØŌČ╚×ķ0.99Ī┴10-3 mg ĪżL-1Ż¼│²┴ūąį─▄ķ_╩╝│÷¼F╩▄ęųųŲ¼FŽ¾Ż¼▒Ē¼F×ķģÆč§─®Č╦┴ūØŌČ╚ĮĄų┴25.13 mg ĪżL-1Ūę║├č§ļAČ╬╬³┴ū─▄┴”£p╚§Ż¼Ę┤æ¬ĮY╩°Ģr╚įėą2.33 mg ĪżL-1Ą─PO43--PÜł┴¶. ▀Mę╗▓Į╝ė┤¾NO2--N═Č╝ė┴┐ų┴15 mg ĪżL-1║═20 mg ĪżL-1(╣żør5Ż¼6)Ż¼╝┤FNA×ķ1.46Ī┴10-3 mg ĪżL-1║═1.94Ī┴10-3 mg ĪżL-1Ż¼ęųųŲ¼FŽ¾Ė³╝ė├„’@Ż¼ģÆč§ßī┴ū┴┐╝░║├č§╬³┴ū┴┐▀Mę╗▓Į£p╔┘Ż¼ŪꎥĮyā╚NO3--NĄ─Ęe└█┴┐ų▓Į╠ßĖ▀.
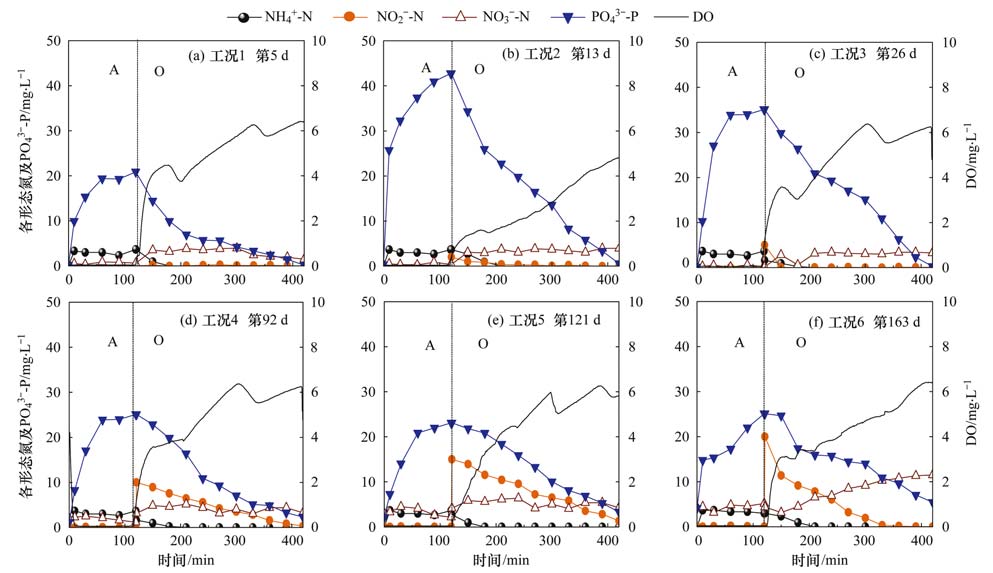
ĪĪĪĪłD 4 ▓╗═¼FNAØŌČ╚Ž┬Ąõą═ų▄Ų┌ā╚Ė„ą╬æBĄ¬╝░PO43--PĄ─ØŌČ╚ūā╗»ęÄ┬╔
ĪĪĪĪ2.3 ▓╗═¼ØŌČ╚FNAī”ŽĄĮy▒╚ßī/╬³┴ū╦┘┬╩Ą─ė░Ēæ
ĪĪĪĪłD 5×ķ▓╗═¼FNAØŌČ╚Ž┬Ż¼Ė„╣żørĘĆČ©▀\ąąĢrŽĄĮyĄ─▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩. Å─ųą┐╔ęŖŻ¼═Č╝ėFNA║¾Ż¼Ę┤æ¬Ų„╗ņ║Žę║Ą─▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩Š∙Ė▀ė┌═Č╝ėŪ░. ĮY║ŽłD 3▓╗ļy░l¼FŻ¼Š█┴ūŠ·Ą─ßī┴ū║═╬³┴ū─▄┴”į┌Č╠Ų┌ā╚Ģ■╩▄ĄĮFNAęųųŲŻ¼Č°ķLŲ┌▀\ąąŲõ╗ŅąįĢ■ų▓Į╗ųÅ═Ż¼ė╔┤╦═Ų£yŻ¼PAOs┐╔─▄╩ŪĮĶ▀ĆįŁü厧╦ß¹}ė├ęįĮŌČŠ. ī”Ė„ØŌČ╚Śl╝■Ž┬Ą─▒╚Ę┤æ¬╦┘┬╩Ū·ŠĆöM║Ž░l¼FŻ¼ļSų°FNAØŌČ╚Ą─į÷Ė▀Ż¼ŽĄĮy▒╚ßī/╬³┴ū╦┘┬╩│╩¼FŽ╚į÷┤¾║¾£pąĪĄ─Æü╬’ŠĆ┌ģä▌Ż¼šf├„Ą═ØŌČ╚Ą─FNA(<0.99Ī┴10-3 mg ĪżL-1)▓╗āH╬┤ęųųŲ╬█─ÓĄ─ßī┴ū╝░╬³┴ū─▄┴”Ż¼Ę┤Č°ŲĄĮ┴╦┤┘▀Mū„ė├Ż¼▀@ę╗¼FŽ¾┐╔ęįė╔FNAĄ─ĮŌ±Ņ┬ōū„ė├ĮŌßī. ═©▀^ī”¤╔╣Ō╝┘å╬░¹Š·Ą─蹊┐Ż¼čąŠ┐š▀ūCīŹ┴╦FNA┐╔ęįū„×ķ┘|ūė▌d¾w═Ė▀^╝Ü░¹─żŪęį┌─żā╔é╚═∙Å═▀\äėČ°▓╗«a╔·─▄┴┐[25, 26, 27]Ż¼Ą½FNAĄ─ĮŌ┼╝┬ōū„ė├ī¦ų┬Ųõ═Ė▀^╝Ü░¹─ż║¾░¹═Ō“īäė┘|ūėĄ──▄┴┐į÷╝ėŻ¼ę“┤╦Ż¼PAOs▒žĒÜ╠ßĖ▀║¶╬³╦┘┬╩Ż¼╝┤ĘųĮŌĖ³ČÓĄ─Š█┴ū(Poly-P)ęį▒├│÷Ė³ČÓ┘|ūėÅ─Č°ŠS│ų┘|ūė“īäė┴”Ą─║ŃČ©[28]. ī”łD 5Ą─Ęų╬÷▀Ć░l¼FŻ¼▒╚ßī┴ū╦┘┬╩Ą─ś╦£╩Ų½▓ŅĘČć·Š∙┤¾ė┌▒╚╬³┴ū╦┘┬╩Ą─ś╦£╩Ų½▓ŅĘČć·Ż¼Ūę▒╚ßī┴ū╦┘┬╩Ą─Ū·ŠĆūā╗»┌ģä▌├„’@Ż¼šf├„FNAī”ģÆč§Ę┼┴ūĄ─ė░Ēæ┤¾ė┌║├č§╬³┴ū.
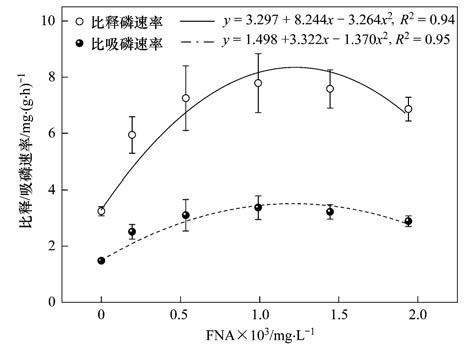
ĪĪĪĪłD 5 ▓╗═¼FNAØŌČ╚Ž┬ŽĄĮyĄ─▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩
ĪĪĪĪFNAØŌČ╚Ė▀ė┌0.99Ī┴10-3 mg ĪżL-1║¾Ż¼ŽĄĮy▒╚ßī/╬³┴ū╦┘┬╩│╩¼F┬į£p┌ģä▌. ėąīWš▀╠ß│÷Ż¼╚ń╣¹PAOs¾wā╚Ą─ü厧╦ß¹}▀ĆįŁ├Ė(nir)į┌║├觌l╝■Ž┬─▄īóNO2-ę└┤╬▀ĆįŁ×ķNOĪó N2O║═N2Ż¼Č°NO2-╗“NOėų┼cč§╗»▀ĆįŁ├ĖĘ┤æ¬Ż¼Ųõ«a╬’Ģ■ęųųŲPAOsĄ─║├č§║¶╬³Ż¼Å─Č°ęųųŲ─▄┴┐«a╔·Ż¼╩╣PAOs¾wā╚╠ŪįŁ║═Poly-PĄ─║Ž│╔ęį╝░╝Ü░¹Ą─╔·ķL╩▄ĄĮė░Ēæ[29]. ▒M╣▄╚ń┤╦Ż¼ŲõšµīŹĄ─ÖCųŲ╔ą▓╗ŪÕ│■Ż¼ę“┤╦Ż¼ėąĻPFNAī”Š█┴ūŠ·║├č§╬³┴ūĄ─ęųųŲÖCųŲėą┤²▀Mę╗▓Į蹊┐.
ĪĪĪĪ2.4 ═Č╝ėFNAŪ░║¾╬█─Ó╚▒č§╬³┴ū─▄┴”Ą─ūā╗»
ĪĪĪĪłD 6×ķŽĄĮy═Č╝ėFNAŪ░║¾ęįNO2-║═NO3-×ķļŖūė╩▄¾wĄ─╚▒č§╬³┴ūįć“×ųąPO43--P║═NOx--NĄ─ūā╗»ęÄ┬╔. ī”łD 6(a) ųąā╔ĘNļŖūė╩▄¾w╬³┴ūŪ·ŠĆ▀MąąŠĆąįöM║Ž▓óĘų╬÷┐╔ų¬Ż¼±Z╗»Ū░Ż¼ŽĄĮyęįNO2-║═NO3-×ķļŖūė╩▄¾wĄ─Ę┤Ž§╗»╬³┴ūŠ∙─▄▀MąąŻ¼Ą½NO3-ą═Ą─▒╚╬³┴ū╦┘┬╩(ęįVSSėŗŻ¼Ž┬═¼)×ķ7.95 mg Īż(g Īżh)-1╝░ļŖūė╩▄¾w▒╚└¹ė├╦┘┬╩×ķ5.33 mg Īż(g Īżh)-1┬įĖ▀ė┌NO2-ą═Ą─▒╚╬³┴ū╦┘┬╩×ķ7.32 mg Īż(g Īżh)-1╝░ļŖūė╩▄¾w▒╚└¹ė├╦┘┬╩5.06 mg Īż(g Īżh)-1Ż¼Č°ŪęŻ¼įć“×ĮY╩°ĢrŽĄĮyųą╚įėą╔┘┴┐PO43--P║═ļŖūė╩▄¾w┤µį┌. ═Č╝ėFNA±Z╗»65 d║¾Ż¼ī”łD 6(b)Ą─Ęų╬÷░l¼FŻ¼ā╔ĘNŅÉą═╚▒č§╬³┴ūĄ─╬³┴ū╦┘┬╩║═ļŖūė╩▄¾w└¹ė├╦┘┬╩Š∙ėą┤¾Ę∙╠ß╔²Ūę╬█─ÓĄ─╚▒č§╬³┴ūĘĮ╩Į░l╔·▐DūāŻ¼NO3-ą═Ą─▒╚╬³┴ū╦┘┬╩26.64 mg Īż(g Īżh)-1 ╝░ļŖūė╩▄¾w▒╚└¹ė├╦┘┬╩12.75 mg Īż(g Īżh)-1 Š∙ąĪė┌NO2-ą═Ą─▒╚╬³┴ū╦┘┬╩28.25 mg Īż(g Īżh)-1╝░ļŖūė╩▄¾w▒╚└¹ė├╦┘┬╩14.07 mg Īż(g Īżh)-1Ż¼╚▒č§╬³┴ū─▄┴”Ęųäe×ķ±Z╗»Ū░Ą─3.35▒Č║═3.86▒Č. ╔Ž╩÷¼FŽ¾šf├„Ż¼Ž“║├č§╬³┴ūŽĄĮyā╚═Č╝ėFNA▓óķLŲ┌±Z╗»ėą└¹ė┌ŽĄĮyā╚║Y▀xŠ▀ėąęįNO2-×ķļŖūė╩▄¾wĄ─Ę┤Ž§╗»Š█┴ūŠ·.
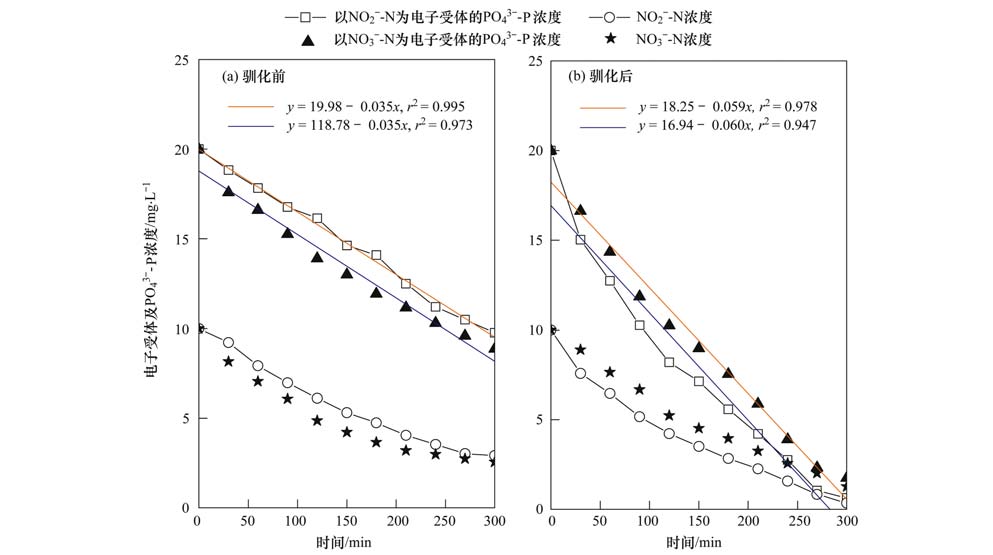
ĪĪĪĪłD 6 FNA±Z╗»Ū░║¾╬█─ÓĄ─╚▒č§╬³┴ū─▄┴”
ĪĪĪĪ2.5 ▓╗═¼FNAØŌČ╚Ž┬Ą─ŽĄĮy╬█─Ó┴┐╝░Ųõ│┴ĮĄąį─▄
ĪĪĪĪłD 7×ķFNA═Č╝ė┴┐ī”ŽĄĮyā╚╬█─Ó┴┐╝░Ųõ│┴ĮĄąį─▄Ą─ė░Ēæ. Å─ųąĘų╬÷┐╔ų¬Ż¼įć“×▀MąąĄ─Ū░20 dŻ¼ŽĄĮy╗ņ║Žę║Ą─MLSSųĄė╔4 963 mg ĪżL-1ĮĄų┴3 000 mg ĪżL-1ū¾ėę. Ęų╬÷įŁę“Ż¼FNAĄ─ęųųŲū„ė├ų┬╩╣▓┐Ęų╬ó╔·╬’▒╗Üó£ń╗“╝Ü░¹į÷ų│┴┐Ą═ė┌┼┼─Ó┴┐Ż¼╚╗Č°Ż¼Įø▀^ę╗Č╬Ģrķg║¾Ż¼ė╚Ųõ╩Ū═Č╝ė0.99Ī┴10-3 mg ĪżL-1Ą─FNA║¾╬█─ÓØŌČ╚┌ģė┌ŲĮĘĆŻ¼šf├„ŽĄĮyā╚╬█─Ó▀M╚ļ▀mæ¬Ų┌. ė╔▓╗═¼FNAØŌČ╚Ž┬Ę┤æ¬Ų„ā╚╬█─Ó¾wĘeųĖöĄ(SVI)Ą─ūā╗»┐╔ęŖŻ¼ļSų°įć“ץ─▀MąąŻ¼SVIų▓ĮĮĄĄ═ų▒ų┴ĘĆČ©Ż¼▀@┼c╬█─ÓØŌČ╚ūā╗»┌ģä▌ę╗ų┬. Ęų╬÷įŁę“Ż║ ę╗ĘĮ├µŻ¼FNAęųųŲ┴╦ĮzĀŅŠ·Ą─╔·ķL; ┴Ēę╗ĘĮ├µŻ¼łD 4’@╩ŠĄ─▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩Ą─į÷┤¾▒Ē├„PAOs╗Ņąįį÷ÅŖ╗“öĄ┴┐į÷ČÓŻ¼ę“Č°╗Ņąį╬█─Ó▒╚ųž▌^┤¾Ż¼Ė³ėą└¹ė┌╬█─ÓĄ─│┴ĮĄ.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.bnynw.comĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
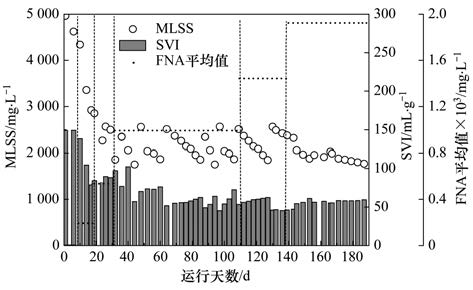
ĪĪĪĪłD 7 FNAī”ŽĄĮy╬█─Ó┴┐╝░Ųõ│┴ĮĄąį─▄Ą─ė░Ēæ
ĪĪĪĪ3 ĮYšō
ĪĪĪĪ(1)FNA×ķ0-1.46Ī┴10-3 mg ĪżL-1ØŌČ╚ĘČć·ā╚Ż¼│÷╦«¤oNO2--NĘe└█Ż¼NO3--NĘe└█┴┐ļSų°FNA═Č╝ė┴┐Ą─į÷┤¾Č°į÷ČÓŻ¼┐饬ōp╩¦┬╩Š∙Ė▀ė┌80%Ż¼NO2--Nōp╩¦┴┐ė╔0 mg ĪżL-1╔²ų┴11.495 mg ĪżL-1Ż¼FNA×ķ1.94Ī┴10-3mg ĪżL-1ĢrŻ¼ŽĄĮyā╚ų▓Į│÷¼FNO2--NĄ─Ęe└█.
ĪĪĪĪ(2)═Č╝ėFNA║¾╬█─ÓĄ─ßī┴ū║═╬³┴ū─▄┴”▓╗āH╬┤╩▄ĄĮęųųŲŻ¼▒╚ßī┴ū╦┘┬╩║═▒╚╬³┴ū╦┘┬╩Ę┤Č°Ė▀ė┌═Č╝ėŪ░. FNAĄ═ė┌0.53Ī┴10-3 mg ĪżL-1ĢrŻ¼ŽĄĮy│²┴ū┬╩Š∙┤¾ė┌96.9%; «öFNAØŌČ╚╠ßĖ▀ų┴0.99Ī┴10-3Īó 1.46Ī┴10-3Īó 1.94Ī┴10-3 mg ĪżL-1ĢrŻ¼│²┴ū┬╩Š∙ėą┤¾Ę∙Ž┬ĮĄŻ¼ĘųäeĮø▀^50Īó 12Īó 30 dĄ─▀\ąąŻ¼│²┴ūąį─▄╗ųÅ═ų┴64.42%Īó 67.33%Īó 44.14%Ż¼šf├„ęųųŲū„ė├ī¦ų┬Ą─│²┴ūąį─▄É║╗»┐╔ęį╗ųÅ═ŪęķLŲ┌±Z╗»ū„ė├─▄┐sČ╠╗ųÅ═▀^│╠.
ĪĪĪĪ(3)═Č╝ėFNA±Z╗»║¾Ż¼╬█─ÓĄ─NO3-ą═║═NO2-ą═╚▒č§╬³┴ū─▄┴”Ęųäe×ķ±Z╗»Ū░Ą─3.35▒Č║═3.86▒ČŪę╬³┴ūĘĮ╩Įėą╦∙▐DūāŻ¼šf├„Ž“║├č§╬³┴ūŽĄĮyā╚ķLŲ┌═Č╝ėFNAėą└¹ė┌ŽĄĮyā╚Ė╗╝»ęįNO2-×ķļŖūė╩▄¾wĄ─Ę┤Ž§╗»Š█┴ūŠ·; Č°ŪęŻ¼ķLŲ┌±Z╗»▀^│╠ėą└¹ė┌ŽĄĮyā╚╬█─ÓĄ─│┴ĮĄ.Ż©üĒį┤╝░ū„š▀Ż║ ╠mų▌Į╗═©┤¾īWŁhŠ│┼c╩ąš■╣ż│╠īWį║ ±RŠĻ └ŅĶ┤ ėßąĪ▄Ŗ īO└ū▄Ŗ īO║ķéź ĻÉė└ųŠŻ®


